على آلية خفية تسمح لخلايا الجهاز العصبي المحيطي بالتعافي بسرعة بعد الإصابة
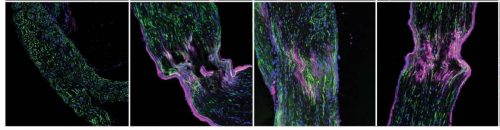
عندما يحتاج جسمنا إلى إصلاح العصب التالف في الجهاز العصبي المحيطي، فإن جميع الأدوات اللازمة تكون موجودة بالفعل في المكان المناسب: يمكن للمفتاح الجزيئي المخفي أن يزيد، إذا لزم الأمر، إنتاج البروتينات في المنطقة المتضررة بالضبط، مما يتيح التعافي. وفي دراسة نشرت مؤخرا في المجلة العلمية Science، اكتشف علماء معهد وايزمان للعلوم وشركاؤهم في البحث كيفية عمل هذه الآلية. تسلط النتائج التي توصلوا إليها ضوءًا جديدًا على نمو الخلايا وإصلاحها، وتشير إلى الاتجاهات المحتملة لتطوير الأدوية.
أراد العلماء في مجموعة البروفيسور مايك فينزيلفر، في قسم العلوم الجزيئية الحيوية، معرفة دور البروتين المسمى mTOR في شفاء الأعصاب. "يذكرنا البروتين بـ "الحلقة الواحدة" - تلك التي تحكم جميع الحلقات الأخرى - من كتاب جيه آر. تولكين "سيد الخواتم"، يشرح البروفيسور فينزلبر النتائج من خلال قصة رمزية أدبية. "ليس فقط لأن البروتين هو المسؤول عن التحكم العام في إنتاج البروتينات في الجسم ونمو الخلايا العصبية، ولكن أيضًا، كما اتضح لنا، لأنه يشبه "الحلقة الواحدة" فإنه يمكن أن يختبئ ويأتي إلى العمل إذا لزم الأمر في الوقت والمكان المناسبين."
اكتشف الدكتور ماركو تيرينزيو وأعضاء آخرون في مجموعة البروفيسور فينسيلفر البروتين في موقع الإصابة في العصب الوركي لدى الفئران. وتفاجأ العلماء بالسرعة التي ظهرت بها جزيئاته في مكان الإصابة، فهو عصب طويل للغاية يتكون من خلايا عصبية في أسفل الظهر تصل امتداداتها، أي المحاور، إلى القدم. وإذا تم إنتاج الجزيئات في الخلايا العصبية لأجسامهم، فسيستغرق الأمر حوالي نصف يوم للوصول إلى موقع الإصابة في منطقة منتصف الفخذ. وبما أنه تم قياس الزيادة الحادة في مستوى البروتين بعد ساعتين إلى ثلاث ساعات من لحظة الإصابة، فقد خلص العلماء إلى أن بروتين mTOR تم إنتاجه بطريقة أو بأخرى في نفس المكان.
وبمساعدة نسخة متقدمة من قياس الطيف الكتلي، والتي تجعل من الممكن التعرف في الوقت الحقيقي على البروتينات الجديدة المنتجة في الأنسجة الحية، وجد العلماء - بالتعاون مع مجموعة البروفيسور ألما بيرلينجهايم من جامعة كاليفورنيا، سان فرانسيسكو - أنه بعد إصابة العصب، يشجع البروتين mTOR إنتاجه الخاص، كما أن مستوياته العالية في حد ذاتها تشجع الإنتاج المحلي لبروتينات أخرى ضرورية لبقاء العصب وإصلاحه. وهكذا، عندما منع العلماء إنتاج mTOR بعد الإصابة، لم يتم إنتاج أي بروتينات أخرى تقريبًا في المحور العصبي التالف.
ويذكرنا البروتين بـ "الحلقة الواحدة" من كتاب "سيد الخواتم". ليس فقط لأن البروتين مسؤول عن التحكم العام في إنتاج البروتين ونمو الخلايا العصبية، ولكن أيضًا لأنه، على غرار "الحلقة الواحدة"، يمكن أن يختبئ ويبدأ العمل إذا لزم الأمر في الوقت والمكان المناسبين.

الواقفون من اليمين إلى اليسار: إيلا دورون ماندل، د. إيدا ريشيل، د. سانديب كولي، البروفيسور مايك فينزلفر، د. إندراك كوبيل، د. ماركو تيرينزيو. الجالسون من اليمين إلى اليسار: د. روتام بن توف بيري، نيتسان سمارا، أوجستينا دي فيزيو، د. ليتيتيا ماربليدي
الواقفون من اليمين إلى اليسار: إيلا دورون ماندل، د. إيدا ريشيل، د. سانديب كولي، البروفيسور مايك فينزلفر، د. إندراك كوبيل، د. ماركو تيرينزيو. الجالسون من اليمين إلى اليسار: د. روتيم بن توف بيري، نيتسان سمارة، أوجستينا دي فيزي... شاهد المزيد
ولكن ما الذي يسبب الزيادة في مستويات mTOR نفسها؟ وبالتعاون مع مختبر البروفيسور جيفري تويس من جامعة كارولينا الجنوبية، اكتشف العلماء أنه حتى في الحالة الطبيعية، عندما لا تكون هناك إصابة، هناك "تعليمات" لإنتاج mTOR: جزيئات RNA المرسال التي تحمل المادة. "وصفة" وراثية لبناء هذا البروتين على طول المحور العصبي. وتنتشر هذه الجزيئات على طول المحور العصبي لضمان تواجدها في المكان المطلوب عند الحاجة إليها. وهكذا، عند تلف العصب، يمكنك "تشمر عن سواعدك" والبدء على الفور في إنتاج mTOR اللازم للإصلاح. وللتحقق مما إذا كانت هذه هي الطريقة التي تعمل بها الآلية، قام العلماء - باستخدام تقنية تحرير الجينات - بإزالة جزء من جزيئات الحمض النووي الريبي المرسال الذي يسمح بالنقل إلى المحور العصبي. ونتيجة لذلك، لم يحدث إنتاج البروتين في المحور العصبي، ولم تنجو الخلايا العصبية من الإصابة.
يوضح البروفيسور فاينزلبر: "تمامًا كما يمكن أن تسبب "الحلقة الواحدة" لتولكين مشكلة إذا كانت في الأيدي الخطأ، كذلك يمكن لـ mTOR أيضًا تعطيل العمليات إذا تم تنشيطها في الوقت الخطأ أو في المكان الخطأ في الخلية. على سبيل المثال، قد يسبب الألم بسبب نمو الأعصاب غير المنضبط أو السرطان الناتج عن نمو الخلايا المفرط. ومن ناحية أخرى، فإن إنتاج mTOR في الزمان والمكان المطلوبين - وفي الزمان والمكان المطلوبين فقط - وفقًا لتعليمات الحمض النووي الريبوزي الرسول الموجود، يعد طريقة سريعة وآمنة للتوصيل المتحكم لهذا البروتين. "
ربما تكون هذه الآلية مسؤولة عن إنتاج mTOR ليس فقط في حالات الإصابة، ولكن في مجموعة متنوعة من العمليات الخلوية الأخرى، بما في ذلك تشجيع نمو الخلايا العصبية في جسم الإنسان في العقدين الأولين من الحياة. ومن ناحية أخرى، من المعروف أن العيوب في نشاط mTOR لها دور في العديد من الأمراض، بما في ذلك السرطان والسكري والسمنة. توجد حاليًا أدوية في السوق تمنع نشاط هذا البروتين، لكن الكشف عن الآلية الخفية لإنتاج mTOR قد يجعل من الممكن تطوير أدوية جديدة تتحكم في نشاط البروتين في حالات المرض والإصابات.
كما شارك في المؤتمر كل من الدكتور سانديب كولي، نيتسان سمارا، الدكتورة إيدا ريشيل، الدكتورة ليتيسيا ماربليدي، أوجستينا دي فيزيو، إيلا دورون ميندل، الدكتور روتام بن توف بيري والدكتور إندراك كوبيل، وجميعهم من قسم العلوم الجزيئية الحيوية. الدراسة. .
#أرقام_علمية
يحتوي ترميز الحمض النووي الريبوزي (RNA) لبروتين mTOR على حوالي 8,700 قاعدة، منها 7,650 قاعدة مشفرة للبروتين، والباقي عبارة عن "ذيول غير مترجمة" تلعب أدوار تحكم مختلفة. في "الذيل الخلفي"، 825 قاعدة بما في ذلك تسلسل يرتبط بالبروتينات التي تنقل الحمض النووي الريبي (RNA) إلى امتدادات الخلايا العصبية.
المزيد عن الموضوع على موقع العلوم:
