وتبين أن قدرة الأورام السرطانية على التطور ترجع إلى الخصائص الفريدة للخلايا الجذعية السرطانية الموجودة فيها

إلى جانب دراسة الخلايا الجذعية الجنينية، التي تتكون منها جميع أنسجة الجسم في المراحل المبكرة من النمو، فقد تزايد الاهتمام مؤخرًا بالخلايا الجذعية البالغة التي يتمثل دورها في "الحفاظ" على الأنسجة الموجودة أثناء الحياة - أي تكوينها. خلايا جديدة بدلا من الخلايا الميتة. وتتميز الخلايا الجذعية الناضجة بميزات فريدة تتيح لها القيام بأعمال الصيانة: القدرة على التجديد الذاتي، وتأخر عمليات التمايز الخلوي. ولكن اتضح أن نفس الخصائص تجعلها مرشحة جيدة لتصبح خلايا سرطانية. ويزعم العديد من العلماء مؤخرا أن أصل الأورام السرطانية عادة ما يكون في الخلايا الجذعية الناضجة التي أصبحت سرطانية. ووفقا لهذه النظرية، عندما تخضع الخلية الجذعية البالغة لتغيرات جينية، فإنها قد تفقد آليات التحكم الخاصة بها وتتحول إلى خلية سرطانية، مع احتفاظها بخصائص التجديد الذاتي للخلية الجذعية. وهذا المزيج بين خصائص الخلية الجذعية والخصائص السرطانية هو ما يؤدي إلى تطور الورم السرطاني.
وقد ثبت في العقد الأخير أن العديد من الأورام السرطانية (مثل سرطان الدم وسرطان الثدي وأورام المخ) تحتوي أيضًا على كمية صغيرة من الخلايا الجذعية السرطانية، وهي المسؤولة عن التجدد المستمر للخلايا السرطانية. وتشير هذه النتائج إلى أنه من أجل القضاء على الورم بشكل كامل، ومنع ظهوره مرة أخرى، يجب تدمير الخلايا الجذعية السرطانية بالكامل. ولسوء الحظ، فقد تبين أنه في كثير من الحالات تكون هذه الخلايا مقاومة للعلاجات الكيميائية المقبولة حاليا. وتسمح لهم هذه المقاومة بالبقاء على قيد الحياة، وتتسبب في عودة المرض لدى المرضى الذين عولجوا بالعلاج الكيميائي وتعافوا.
كيفية تدمير الخلايا الجذعية السرطانية؟ تتطلب الإجابة على هذا السؤال التوصيف الجيني للخلية الجذعية السرطانية، ومعرفة نمط التعبير البروتيني الخاص بها، وفهم أسباب العملية التي تحول الخلية الجذعية البالغة السليمة إلى خلية سرطانية. كان هذا الموضوع في قلب البحث الذي أجراه مؤخراً البروفيسور ديفيد غافول وطالبة البحث هيلا غال من قسم البيولوجيا الجزيئية للخلية، بالتعاون مع البروفيسور تسفي لابيدوت من قسم علم المناعة والبروفيسور إيتان دوماني من قسم علم المناعة. قسم فيزياء الأنظمة المعقدة. كما شارك في المؤتمر أعضاء فريق البحث للبروفيسور جدعون رفافي من المركز الطبي شيبا في تل هشومير.
قدمت دراسة الخلايا المشاركة في تكوين ورم سرطان الدم، سرطان الدم، أحد الأدلة الأولى على وجود الخلايا الجذعية السرطانية. في هذه الدراسات، تمكن الباحثون من التمييز بين مجموعتين من الخلايا السرطانية: في مجموعة واحدة (الأصغر) كانت هناك خلايا، عند حقنها في حيوانات التجارب، كانت قادرة على التسبب في تطور سرطان الدم في الحيوان المتلقي. المجموعة الثانية (الأكبر) كانت لديها خلايا ناضجة فقدت القدرة على التجدد، ولم يتسبب حقنها في حيوانات التجارب في تطور سرطان الدم لدى الحيوان المتلقي.
تشترك خلايا المجموعة الأولى في خصائص مشتركة مع الخلايا الجذعية السليمة، مما أدى إلى افتراض أن الخلايا الجذعية السرطانية، التي تولد من الخلايا الجذعية لجهاز الدم، هي المسؤولة عن تطور سرطان الدم. وفي دراسة نشرت مؤخرا في مجلة سرطان الدم، قارن العلماء المظهر الجيني للخلايا الجذعية لسرطان الدم مع تلك الموجودة في خلايا سرطان الدم غير الجذعية، وحددوا حوالي 400 جين تختلف درجة تعبيرهم. وهكذا، على سبيل المثال، أظهرت الخلايا الجذعية السرطانية انخفاضا في التعبير عن الجينات المرتبطة بتصحيح الأخطاء في تسلسل الحمض النووي، وهو ما قد يفسر حقيقة أنها أكثر عرضة لتراكم الطفرات الضارة. وأظهر فحص تعبير هذه الجينات الـ400 في الخلايا الجذعية السليمة لجهاز الدم، أن ثلثها مشترك بين مجموعتي الخلايا الجذعية، مما يعزز نظرية الأصل المشترك لنوعي الخلايا. وهكذا، على سبيل المثال، تم العثور على مسار داخل الخلايا لنقل الإشارات، والذي يزداد التعبير عنه في كلا النوعين من الخلايا الجذعية. وتمكن الباحثون من تثبيط المسار، وبالتالي تحقيق انخفاض في معدل انقسام الخلايا الجذعية في المزرعة - سواء السرطانية أو البالغة. إن تحديد المسارات المتعلقة بآلية الانقسام والتجديد الذاتي للخلايا الجذعية السرطانية هو الخطوة الأولى على طريق تطوير الأدوية التي من شأنها سد هذه المسارات، ووقف تطور الورم. ويتمثل التحدي التالي في تحديد المسارات التي تميز الخلايا الجذعية السرطانية، بحيث لا يؤدي تلفها إلى الإضرار بالخلايا الجذعية السليمة، ولا يتعارض مع الصيانة المستمرة للأنسجة السليمة.
وفي الدراسة الحالية، تم اكتشاف أن أكثر من نصف الجينات المعبر عنها في الخلايا الجذعية السرطانية لا تتم مشاركتها مع الخلايا الجذعية السليمة، وبالتالي يمكن استخدامها كهدف للقضاء الانتقائي على الخلايا الجذعية السرطانية. البروفيسور جافول: "النجاح في هذا المجال سيمكن من تحديد المكونات الفريدة للخلايا الجذعية السرطانية. العلاجات الدوائية التي تستهدف هذه المكونات الفريدة ستمكن من إحداث ضرر انتقائي للخلايا الجذعية السرطانية، مع تجنب الضرر غير المرغوب فيه للخلايا الجذعية السليمة.
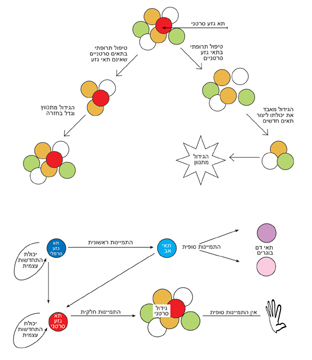
يؤدي العلاج المقبول حاليًا إلى تدمير معظم الخلايا السرطانية، مما يؤدي إلى انكماش الورم. لكن الخلايا الجذعية السرطانية تقاوم هذا العلاج في الغالب، مما يتسبب في إعادة نمو الورم. العلاج الذي من شأنه أن يدمر الخلايا الجذعية السرطانية سيمنع الورم من الظهور مرة أخرى، وسيسمح بالشفاء التام.