اكتشف باحثون من جامعة رايس أن قطع بروتين فلوري معين واستخدامه كعلامة مناسب لفحص نشاط الخلايا الحية
نصف البروتين أفضل من لا شيء، وفي حالتنا أفضل من البروتين الكامل. اكتشف باحثون من جامعة رايس أن قطع بروتين مفلور معين واستخدامه كعلامة مناسب لفحص نشاط الخلايا الحية، خاصة في فهم الطريقة التي تستخدم بها تراكمات كبريتيد الحديد.
الحديد والكبريت بكميات مناسبة ضرورية لصحة جيدة. توجد هذه العناصر في الطعام الذي يتناوله الأشخاص وفي الفيتامينات التي يستهلكونها يوميًا، ولكن وجودها كثيرًا أو قليلًا جدًا في الخلايا يمكن أن يسبب مشاكل صحية خطيرة.
مجموعات الحديد والكبريت هي مركبات تحتوي على أربع ذرات على الأقل. يتم إنتاجها وتنظيمها في الخلايا الحية بواسطة البروتينات، ويعد دورها مجالًا بحثيًا جديدًا نسبيًا للباحثين المهتمين بفهم الأمراض الناجمة عن عيوب في البروتينات (ترنح فريدريك، وفقر الدم الحديدي الأرومات، والاعتلال العضلي). ومع ذلك، حتى الآن لم تكن هناك طريقة لمراقبة هذه التجمعات المعدنية في الخلايا الحية.
وقد قام الباحث جوناثان سيلبيرج، أستاذ الكيمياء الحيوية وبيولوجيا الخلية بجامعة رايس، بدراسة أسرار هذه الفراء لسنوات. لقد وجد طريقة لمعرفة كيفية عملها في الخلايا الحية. ونشر الباحث وفريقه مقالاً في المجلة العلمية Chemistry & Biology يصف تفاصيل الطريقة الجديدة التي تمكن من تصوير الركام من خلال ربطها بقطعة بروتين فلوري وسيطة.
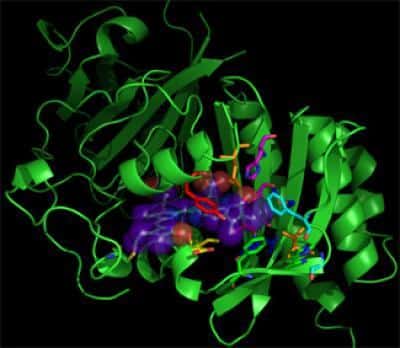
الوسيط هو بروتين بشري يعرف باسم GRX2، وهو إنزيم مؤكسد من نوع الجلوتاروكسين، يساعد الخلايا على التعامل مع الأضرار التأكسدية التي تسببها البروتينات الأخرى في الخلية. ويمكن "إيقاف" نشاطه في المختبر عن طريق ربطه بحوض من الحديد والكبريت. وقد أثبت فريق البحث سابقًا أن هذا البروتين سيظل مرتبطًا بمجموعات كبريت الحديد حتى عند تمييزه ببروتين فلوري أخضر؛ وعلى الرغم من أن النظام مفيد في الاختبارات المختبرية، إلا أن فلورة البروتين لم تكن قوية بما يكفي لرؤيتها في الخلايا الحية.
ومع ذلك، فإن ربط أجزاء من البروتين الفلوري الأصفر، المعروف باسم "فينوس"، بمونومرات البروتين GRX2 كان ناجحًا جدًا. عندما تم حقنها في الخلايا الحية، تم العثور على المونومرات المسمى واستخدمت مجموعات الحديد والكبريت كنوع من الجسر لربطها ببعضها البعض. ونتيجة لذلك، فإن أجزاء البروتين ذات الإشعاع الأصفر تكون قريبة بما يكفي من بعضها البعض لتشع بقوة كافية لرؤيتها تحت المجهر. ويمكن استخدام البروتينات الجديدة لتشخيص الخلايا للكشف عن علامات الأمراض الناجمة عن المخالفات في تركيزات الركام.
"لهذا السبب أنا متحمس للغاية. يقول الباحث: "هذه شاشة ستمكن من تفعيل البيولوجيا الأساسية التي لا يستطيع أحد تفعيلها اليوم". "وهذا النظام لديه إمكانات عالية لمساعدتنا في إيجاد علاجات فعالة ضد الأمراض."
يقول الباحث الرئيسي أن الحديد والكبريت كانا موجودين في "حساء" الأرض البدائي حتى قبل وجود الأكسجين. "عندما تطورت الحياة، كان الغلاف الجوي على الأرض هوائيًا (يفتقر إلى الأكسجين) وكان الحديد والكبريت وفيرًا. من السهل تحضير هذه الركام المعدني، وبالتالي، من السهل أن نتخيل كيف من خلال الكيمياء البسيطة ووفرة هذه الكواشف، ستتطور البروتينات وتستخدم هذه الركام للقيام بالعديد من العمليات الكيميائية.
"ثم تطورت الكائنات الحية التي تقوم بعملية التمثيل الضوئي وبدأت في استهلاك الأكسجين. من السهل جدًا أن يتأكسد الحديد، لذلك طورت الكائنات الحية المناسبة هذه الآلية بأكملها لحمايته وإصلاحه، إذا لزم الأمر. هذه هي بالضبط الآلية التي نحقق فيها".
وتعد القدرة على تتبع هذه التجمعات في الخلايا الحية إنجازًا ذا أهمية كبيرة لجمعية القلب الأمريكية، التي قامت بتمويل جزء من هذا البحث. يقول الباحث الرئيسي: "لقد قدموا لنا التمويل حتى نتمكن من تطوير أدوات إضافية". "إنهم مهتمون بفهم مرض رنح فريدريك (الذي يمكن أن يؤدي إلى أمراض القلب)، لكنهم مهتمون أيضًا بمعرفة ما إذا كان بإمكاننا تطوير طرق إضافية لتصوير البروتينات الأخرى المرتبطة بمجموعات معدنية."
ويوضح في هذه الدراسة: "لقد أجبنا بالفعل على سؤال بيولوجي أساسي - هل تنضم البروتينات من نوع الجلوتاروكسين معًا في الخلايا الحية بواسطة مجموعات معدنية. ولم يُظهر أحد هذا الأمر حتى الآن في الخلايا البشرية الحية. لقد نجحنا في ذلك".
وتوجد الآن أولوية عالية في مختبر الأبحاث لضبط الأدوات الجديدة، ومع ذلك، يشير الباحث إلى أنه يدرك في الطريقة الجديدة إمكانية فحص جذور الشيخوخة نفسها على المدى الطويل. تعتبر الكميات غير الطبيعية من الحديد في جسم الإنسان سامة، وبما أن الأكسدة تبدو سببًا رئيسيًا للشيخوخة، فإن دراسات عمليات الأكسدة تميل إلى جذب الكثير من الاهتمام.
"هل سيشيخ الناس بشكل أسرع لأن مجموعة حمامات الحديد والكبريت لديهم مختلفة؟ في رأيي، الإجابة على هذا السؤال لا تزال بعيدة لعقود من الزمن، لكنه سؤال مثير للاهتمام للغاية - كيف تؤثر التغييرات الصغيرة في الإجهاد التأكسدي على الشيخوخة؟
ويقول: "هذا الأمر أكثر إغراءً اليوم بعد إثبات وجود صلة مباشرة بين العيوب في مجموعة مجموعات كبريت الحديد واستقرار الجينوم النووي". "لم يعد الأمر كما يلي: "أوه، الإجهاد التأكسدي للميتوكوندريا يرتبط بطريقة أو بأخرى بالطفرات في نواة الخلية." هناك أدلة على أن العيوب في مجموعات الحديد والكبريت في الميتوكوندريا قد تكون هذا الارتباط."
