وتم تحويل خلايا الجلد إلى خلايا جذعية قادرة على إنتاج الأنسولين، والذي لن يرفضه الجسم المزروع. هذا الاختراق لديه فرصة لعلاج مرض السكري من النوع الأول في المستقبل
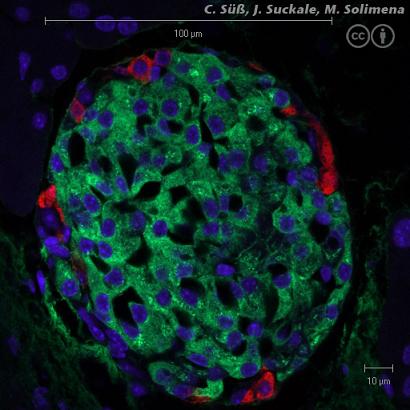
يعد مرض السكري من أكثر الأمراض شيوعًا في المجتمع الغربي المتقدم. ويعاني حوالي 24 مليون أميركي من هذا المرض، الذي ينجم عن عدم قدرة أجسامهم على إنتاج أو استخدام الأنسولين بشكل صحيح. يعتمد جميع مرضى السكري من النوع الأول تقريبًا، وهو الأصعب والأكثر خطورة، على حقن الأنسولين يوميًا لتنظيم مستوى السكر في الدم.
تعتمد الطريقة البديلة لعلاج المرض على زرع خلايا بيتا في البنكرياس يمكنها إنتاج الأنسولين في الجسم بدلاً من الخلايا التي ماتت في جسم المريض. ولسوء الحظ، فإن هذه الخلايا حساسة بشكل خاص للظروف البيئية، وعادة ما تكون هناك حاجة إلى بنكرياسين كاملين، من شخصين مختلفين، لإنتاج خلايا كافية لعملية زرع واحدة.
وبدلاً من خلايا بيتا الناضجة والنادرة، حاول العديد من الباحثين حث الخلايا الجذعية الجنينية على التمايز في المختبر إلى خلايا منتجة للأنسولين. والمشكلة هي أن هذه الخلايا، إذا تم زرعها في المرضى، سوف يتعرف عليها الجهاز المناعي على أنها خلايا غريبة عن الجسم وسيتم مهاجمتها على الفور.
ولحل المشكلة، تعهد باحثون من جامعة نورث كارولينا بإنشاء نوع جديد من الخلايا المنتجة للأنسولين والتي لا يرفضها جسم المتبرع. وفي دراسة نشرت في سبتمبر الماضي، كشف الباحثون عن التقدم الحاصل في هذا المجال، والذي يقول البعض إنه قد يؤدي إلى اختراق حقيقي. خلال البحث، تم أخذ خلايا الجلد البشرية وإخضاعها لعملية أدت إلى فقدانها لوظيفتها وتصبح "خلايا جذعية مستحثة" (خلايا جذعية مستحثة) تشبه في خصائصها الخلايا الجذعية الجنينية. وتم بعد ذلك تمييز الخلايا الجذعية المستحثة إلى خلايا منتجة للأنسولين، في عملية تم عرضها لأول مرة في المختبر.
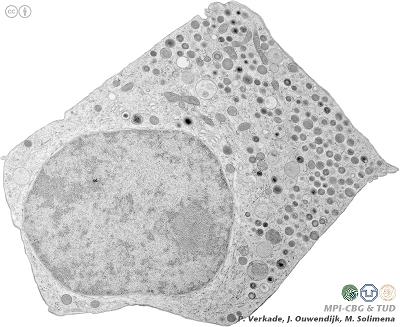
والميزة الكبيرة لهذه الطريقة هي أن خلايا الجلد يمكن أخذها من مريض السكري نفسه، وبالتالي لن يرفضها الجسم حتى عندما تصبح خلايا منتجة للأنسولين ويتم زرعها في جسم المريض. وعلى الرغم من أن تقنية تحويل خلايا الجلد إلى خلايا جذعية قد تم اختراعها بالفعل قبل عامين، إلا أن هذا هو أول دليل على أن الخلايا الجذعية المستحثة يمكنها التمايز إلى خلايا منتجة للأنسولين تساعد في علاج مرض السكري.
على الرغم من أن نتائج الدراسة نُشرت في النسخة الإلكترونية من مجلة الكيمياء البيولوجية، إلا أن باحثين آخرين في هذا المجال يشككون في حجم الإنجاز، ويرجع ذلك أساسًا إلى أن الدراسة الحالية لا تحدد مستوى الأنسولين الذي تمكنت الخلايا الجذعية المنقولة من تحقيقه لانتاج. بالإضافة إلى ذلك، من المعروف أن خلايا بيتا الطبيعية تنتج الأنسولين بمستوى منظم بعناية استجابة لمستوى الجلوكوز في الدم، لكن استجابة الخلايا الجذعية المنقولة للجلوكوز لم يتم تقديرها جيدًا وبالتالي من الصعب استخلاص استنتاجات حول قدرتهم على دخول العيادة في هذه المرحلة.
وعلى الرغم من مشاكل الدراسة، فإن العديد من الأطباء متفائلون بالنتائج. وقال جون بوسا، رئيس الجمعية الأمريكية للسكري وأستاذ ورئيس قسم الغدد الصماء في الجامعة: "بالطبع، ستكون هناك حاجة لسنوات عديدة أخرى من الأبحاث الإضافية، لكن هذه الدراسة توفر الأمل في الدواء لجميع مرضى السكري". من كلية الطب في ولاية كارولينا الشمالية.
من الممكن بل ومن المعقول أن نفترض أننا في بداية عصر جديد، حيث سيتم إيجاد حل مناسب أيضًا للأمراض الوراثية والتمثيل الغذائي. كل ما تبقى هو أن نأمل أن تصل تكنولوجيا الخلايا الجذعية المستحثة إلى مرحلة النضج في غضون سنوات قليلة. ستسمح هذه التكنولوجيا للإنسان بالتغلب على مرض السكري لأول مرة، والذي يتم إجراؤه كاختيار قاس من جانب القدر الأعمى، وستتقدم بالجنس البشري خطوة أخرى على طريق التحكم في مصيره.

تعليقات 10
روعة،
وهذا أمر مستبعد للغاية، لأن البحث الذي أدى إلى إنشاء خلايا جذعية مستحثة لم يُنشر إلا في عام 2006، وأثار ضجة كبيرة. ربما تكون سارة فاربر قد نجحت في جعل خلايا الكبد تنتج الأنسولين، لكن من المشكوك فيه أنها نجحت في تحويلها إلى خلايا جذعية.
إذا كان بإمكانك ربطي بالمقال المعني، فيمكنني الرد بطريقة أكثر استنارة.
شاب شالوم،
روي.
تمكنت باحثة من تل هشومير تدعى سارة فاربر من القيام بنفس الشيء تمامًا منذ حوالي 8 سنوات مع خلايا الكبد فقط وليس خلايا الجلد.
البحث ليس انتهاكا لبراءات الاختراع.
لن يكون هناك مجال للمناقشة حول هذه النقطة إلا إذا تم تطبيق نتائج البحث على الاحتياجات التجارية.
روي
آسف على التأخر في الرد وأشكركم جزيل الشكر على جميع الإجابات.
مقال مثير للاهتمام حقاً، هل هذا يعني أنه لم يعد من الضروري حفظ الدم من الحبل السري من أجل حفظ الخلايا الجذعية للأجنة؟
إذا كانت لدينا القدرة، حتى لو كانت محدودة، على "استعادة" الخلايا لعدة أجيال إلى الخلايا الجذعية المستحثة، فقد يكون هذا حلاً للعديد من المشكلات الأخرى... وليس فقط استعادة خلايا بيتا.
هل من الممكن نظريا زراعة كبد جديد من خلال الخلايا الجذعية المستحثة؟
أعتقد أنني قرأت في مكان ما أنه من الممكن باستخدام الخلايا الجذعية الطبيعية أن تكون قادرًا بطريقة ما على إعادة نمو أجزاء من الكبد فوق ركيزة عندما يكون المصدر من الخلايا الجذعية...
الجليل,
لم أتمكن من العثور على تفاصيل حول تطور (تطورات) Biogenes. لا أعتقد أن هناك أي انتهاك لبراءات الاختراع هنا، حيث أن تقنية إنتاج الخلايا الجذعية المستحثة تم تقديمها منذ عامين فقط. وفقًا لك، كانت شركة Biogenes تعمل في هذا المجال حتى قبل ذلك.
على حد علمي (وقد أكون مخطئًا)، في مجال الطب، يتم التعامل مع الأساليب والأفكار الأقل كبراءات اختراع. أعني أنه يمكنني الحصول على فكرة رائعة للحصول على براءة اختراع (خلايا منتجة للأنسولين في وسط سقالة تحتوي على إنزيمات تعمل على تفكيك النفايات التي تفرزها، لجعل الحياة أسهل بالنسبة لها)، ولكن حتى يكون لدي الحد الأدنى من الدليل على ذلك لقد ابتكرت شيئًا كهذا، ولا فائدة من محاولة تسجيل براءة اختراع له.
الشركة الناشئة التي تسمى Biogenes ومقرها في مشغاف (ابحث على جوجل) كانت تفعل ذلك بالضبط منذ عدة سنوات، فقط مع البروتينات الأساسية الأخرى. أشعر بالفضول لمعرفة ما إذا كان هناك أي انتهاك لبراءات الاختراع الخاصة بهم هنا!
لي،
تم إنشاء الخلايا الجذعية المستحثة من خلايا الجلد المأخوذة من جسم مريض السكري. نظرًا لأن خلايا الجلد الأصلية تحتوي على علامات مناعية تجعل الجهاز المناعي يتعرف عليها كجزء من الجسم، فإن الخلايا الجذعية المستحثة التي تم إنشاؤها منها سيكون لها أيضًا علامات مماثلة. ولهذا السبب، فإنها لن تثير استجابة من الجهاز المناعي إذا تم إعادة حقنها في جسم المريض.
الخلايا الجذعية الجنينية التي يتم أخذها من الجسم البالغ ومن ثم إعادة زرعها داخله، لن تسبب استجابة مناعية أيضًا. لكن لسوء الحظ، لا توجد خلايا جذعية جنينية في جسم الشخص البالغ. ولهذا السبب كان من الضروري استخدام تقنية نقل الخلايا الليفية لإنشاء خلايا جذعية "جنينية" من جسم المريض.
سؤالك الثالث هو على الاطلاق. في كثير من الحالات، يتطور مرض السكري نتيجة لرد فعل مناعي ضد خلايا بيتا في البنكرياس. وحتى في هذه الحالات، يكون الضرر تدريجيًا (واليوم هناك أيضًا تقنيات معروفة لمنعه، بشرط اكتشاف الضرر الأولي في مرحلة مبكرة بما فيه الكفاية). يبدو لي أنهم إذا تمكنوا من إنتاج ما يكفي من خلايا بيتا من الخلايا الجذعية المستحثة، وتمكنوا من ترتيبها في جزر مثل البنكرياس وزرعها بنجاح، فسيكون حل مشكلة المناعة الذاتية سهلاً نسبيًا.
شكرًا على أسئلتك، ويسعدني أن المقال نال اهتمامك.
روي.
ما الفرق بين الخلايا الجذعية المستحثة والخلايا الجذعية الجنينية من وجهة نظر المناعة الذاتية؟
لماذا لا تؤدي الخلايا الجذعية المستحثة إلى استجابة مناعية ذاتية بينما تؤدي الخلايا الجذعية الجنينية إلى استجابة مناعية ذاتية؟
سؤال آخر لدي، حسب ما تعلمته، أحد الأسباب الرئيسية لمرض السكري هو رد فعل المناعة الذاتية الأولي ضد خلايا بيتا في البنكرياس (يعتقد البعض أنه بسبب المواد الحافظة في الهامبرغر والنقانق) وهذا هو السبب في أن الجسم ينتج الأنسولين، فكيف تختلف خلايا بيتا الجديدة عن الخلايا القديمة؟
مثيرة للاهتمام حقا….
المصير العالمي ليس أعمى على الإطلاق.
من الممكن أن يكون المتحدثون عمياء عن رؤيتنا المحيطية - عن حكم الخطة العليا والحياة.
باختصار - بيان مظلم في الأساس.
جور إيل.
الكثير من الدراما، في رأيي، في الفقرة الأخيرة