فرق البحث الإسرائيلية مسؤولة عن إنجازين مهمين في أبحاث علاج مرض باركنسون، باستخدام الخلايا الجذعية الجنينية واستخدام الخلايا الجذعية البالغة
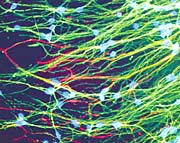
الخلايا العصبية (باللون الأخضر)، تم الحصول عليها بعد تمايز الخلايا الجذعية الجنينية البشرية. تحسنت وظيفة الفئران التي تم زرعها فيها تدريجياً (الصورة: البروفيسور بنجامين روبينوف)
العلماء من إسرائيل هم رواد العالم في مجال أبحاث الخلايا الجذعية - تلك الخلايا القادرة على التمييز والقيام بأدوار الخلايا في أنسجة الجسم المختلفة. وفي الأسبوع الماضي، أعلنت مجموعتان بحثيتان في إسرائيل عن إحراز تقدم كبير في البحث في إمكانية استخدام الخلايا الجذعية لعلاج مرضى باركنسون - وهو المرض الناجم عن انحطاط الخلايا العصبية في منطقة محددة من الدماغ، والتي تفرز مادة تسمى الدوبامين. تمكن باحثون من مركز هداسا عين كارم الطبي من أن يظهروا لأول مرة أن الخلايا الجذعية الجنينية البشرية يمكن أن تحسن وظيفة الفئران المستخدمة كنموذج لمرض باركنسون (أي أولئك الذين يعانون من تلف في الدماغ مماثل لمرضى باركنسون و يعاني من أعراض مشابهة).
نجح فريق بحثي من جامعة تل أبيب لأول مرة في "إقناع" الخلايا الجذعية البشرية الناضجة - تلك القادرة على تغيير غرضها إذا تم تصنيعها للتمايز وزرعها في أنسجة أخرى - لتصبح خلايا منتجة للدوبامين. كما تمكنت أيضًا من إظهار أن الخلايا الجذعية البالغة من الفئران التي خضعت لعلاج مماثل يمكن أن تحسن وظيفة الفئران والجرذان المستخدمة كنموذج لمرض باركنسون.
يقول الدكتور داني أوفين من معهد بلاسينستين للأبحاث الطبية بجامعة تل أبيب: "واحدة من كل ألف خلية نخاع عظمي لديها القدرة على تغيير الغرض". "من أجل استخدام هذه الخلايا لأغراض الزرع، يجب علينا مضاعفتها بشكل كبير في المختبر ومن ثم استخدام أساليب مختلفة من شأنها أن تجبرها على التمايز في الاتجاه المطلوب." واستخدم فريق الباحثين في معهد بلاسنستين، برئاسة البروفيسور إلداد ميلاميد، مدير قسم الأعصاب في مركز رابين الطبي، أساليب طوروها في المختبر لزيادة عدد الخلايا، وكوكتيل خاص يتضمن هرمونات ومكونات مختلفة. عوامل النمو التي وجهت خلايا النخاع العظمي إلى مسار تطوري جديد، حيث أصبحت خلايا مشابهة للخلايا العصبية. يقول ميلاميد: "في غضون فترة قصيرة من الزمن، بدأت الخلايا تظهر خصائص الخلايا العصبية". "لقد قاموا بتطوير امتدادات الأعصاب، والتعبير عن الجينات الفريدة للجهاز العصبي المركزي، وإفراز الدوبامين. وهذه هي المرة الأولى في العالم التي تمكنوا فيها من توجيه تطور الخلايا الجذعية البشرية من نخاع العظم إلى الخلايا العصبية المنتجة للدوبامين في المختبر. تكمن الميزة الكبيرة لاستخدام خلايا نخاع العظم في إمكانية الزرع الذاتي، مما يسمح بتجاوز المشكلات المتعلقة برفض الكسب غير المشروع والآثار الجانبية الأخرى. كما أن هذه الطريقة ليست مفتوحة للاعتراضات من الاعتبارات الأخلاقية."
وفي الوقت نفسه، أجرى الفريق عملًا مشابهًا على الفئران، وتم اتخاذ خطوة أخرى هناك. قام الباحثون بتسمية الخلايا العصبية المنتجة للدوبامين لدى الفئران، والتي تم الحصول عليها من خلايا نخاع العظم، بمادة الفلورسنت، وزرعوها في الفئران والجرذان المستخدمة كنموذج لمرض باركنسون. يقول أوفين: "لقد نجت نسب عالية جدًا من الخلايا في أدمغة الفئران والجرذان لمدة ثلاثة أشهر من المتابعة". "كما رأينا أن الخلايا هاجرت إلى المناطق المتضررة من الدماغ واستقرت هناك، وبعد شهرين أو ثلاثة أشهر شهدنا تحسنا سريريا كبيرا في أداء الحيوانات المريضة. ولأول مرة تمكنا من الحصول على خلايا منتجة للدوبامين في المختبر حلت محل وظيفة الخلايا المنتجة للدوبامين التي ماتت في الدماغ نتيجة المرض". ومن أجل تطوير وتنفيذ الأبحاث من المرحلة المخبرية مروراً بالتجارب السريرية إلى علاج مرضى باركنسون، تم إنشاء شركة تسمى "Brain-Storm"، من خلال شركة "راموت" التابعة لجامعة تل أبيب.
لم يتم الإبلاغ عن أي نجاح في علاج الحيوانات باستخدام الخلايا الجذعية البشرية
تعتبر الخلايا الجذعية الجنينية واعدة في مجال الشفاء الخلوي. ويمكن الحصول عليها بكميات غير محدودة، ونظرًا لكونها خلايا في مراحل مبكرة من التطور، ولم "تلتزم" بعد لغرض محدد، فيمكن التلاعب بها بطرق مختلفة بسهولة أكبر من الخلايا الجذعية الناضجة. وبالتالي فإن التوقعات منهم كثيرة. ومن ناحية أخرى، فإن زرع الخلايا الجذعية الجنينية يثير مشاكله الخاصة. قد تشكل هذه الخلايا أورامًا تسمى الأورام المسخية، والتي تنتج عن الانقسام غير المنضبط للخلايا التي لم تحصل على تصنيف بعد. كما أنه عندما يتعلق الأمر بزراعة الخلايا الجذعية الجنينية، فلا بد من إيجاد حل لمشكلة رفض الخلايا من قبل المريض - وهي مشكلة غير موجودة مع الخلايا الجذعية البالغة، حيث يمكن نقل الخلايا من نخاع عظم المريض إلى المنطقة المتضررة من دماغه.
ومن المعروف بالفعل أنه من الممكن الحصول على الخلايا العصبية المنتجة للدوبامين من الخلايا الجذعية الجنينية للفئران، وزراعتها في أدمغة الفئران المستخدمة كنموذج لمرض باركنسون، وبالتالي علاجها. وأثار نجاح التجربة على الحيوانات الآمال في أن الخلايا الجذعية الجنينية ذات الأصل البشري ستعمل بنفس الطريقة. تحاول العديد من المختبرات حول العالم إنتاج خلايا منتجة للدوبامين من الخلايا الجذعية البشرية، وتشير التقارير الأولية إلى نتائج مشجعة. ولكن لا يزال هناك سؤال حول ما إذا كانت الخلايا الجذعية الجنينية البشرية قادرة، على غرار نظيراتها في الحيوانات، على إحداث تحسن وظيفي في مرض باركنسون. وقد تمكنت مجموعة البحث من هداسا عين كارم من أن تظهر لأول مرة أن هذا هو الحال بالفعل.
يقول البروفيسور بنجامين روبينوف، مدير مركز الأجنة البشرية: "تختلف الخلايا البشرية عن خلايا الفأر من حيث ظروف النمو والخصائص البيولوجية، لذلك ليس من الواضح أنها ستكون قادرة على أداء نفس مهمة الخلايا الجذعية الفأرية". أبحاث الخلايا الجذعية في مركز غولدين سواد للعلاج الوراثي في هداسا عين كارم. "أحد الأشياء المهمة هو إظهار القدرة الوظيفية للخلايا العصبية التي يتم الحصول عليها، ولكن حتى الآن لم يتم الإبلاغ عن نجاح في علاج الحيوانات باستخدام الخلايا الجذعية البشرية." أجرى روبينوف الدراسة مع البروفيسور تامير بن هور من قسم الأعصاب في هداسا. ونشرت النتائج التي توصل إليها في العدد الأخير من مجلة "الخلايا الجذعية".
إعلانات في مختبر روبينوف، تم تطوير طرق فريدة لتوجيه الخلايا الجذعية الجنينية البشرية لتتطور إلى خلايا عصبية بدائية، وأصبح أكثر من 95% من الخلايا المستنبتة خلايا جذعية عصبية. وقام الباحثون بزراعة هذه الخلايا في المنطقة المتضررة من أدمغة الفئران المستخدمة كنموذج لمرض باركنسون، وقاموا بمراقبة سلوك الفئران لمدة ثلاثة أشهر تقريبا. يقول بن هور: "لقد شهدنا تحسنًا تدريجيًا في وظيفة الفئران التي تلقت العلاج مقارنة بالفئران التي لم نزرع الخلايا الجذعية العصبية فيها". "عندما فحصنا ما حدث في أدمغة الفئران، أدركنا أن بعض الخلايا التي زرعناها نضجت داخل الدماغ وتحولت إلى خلايا عصبية منتجة للدوبامين. علاوة على ذلك، رأينا أن هناك علاقة بين عدد الخلايا المنتجة للدوبامين والتحسن في السلوك، مما يعزز الافتراض بأن التحسن في السلوك نتج عن الخلايا التي تم زرعها وأصبحت خلايا منتجة للدوبامين.
ويشير روبينوف إلى أن التحسن السريري في الفئران لم يكن كاملا، لأن عدد الخلايا المنتجة للدوبامين في الدماغ كان صغيرا نسبيا. ويعمل الباحثون الآن على تحسين أساليب إثراء الخلايا التي تنتج الدوبامين، الأمر الذي ربما يجعل من الممكن الحصول على الشفاء التام. ووفقا له، فإن "تطبيق مثل هذا العلاج على المرضى لا يزال أمامه طريق طويل، ومن الصعب تقدير عدد السنوات التي سيستغرقها".
