تمكن باحثون من جامعة هارفارد من إعادة برمجة خلية بنكرياسية ناضجة شائعة في الفئران إلى خلية منتجة للأنسولين تشكل 1% فقط من البنكرياس ولكنها ضرورية للجسم.
هل مجال الأبحاث في مجال الخلايا الجذعية وربما الحاجة إليها على وشك التغيير؟ أفاد باحثون في معهد هارفارد للخلايا الجذعية (HSCI)، بقيادة دوج ميلتون وزميل ما بعد الدكتوراه جو زو، أنهم نجحوا في تحقيق الهدف الذي يحلم به علماء الأحياء التطورية - وهو التحويل المباشر لخلية بالغة من نوع واحد إلى خلية بالغة من الخلايا الجذعية. نوع اخر.
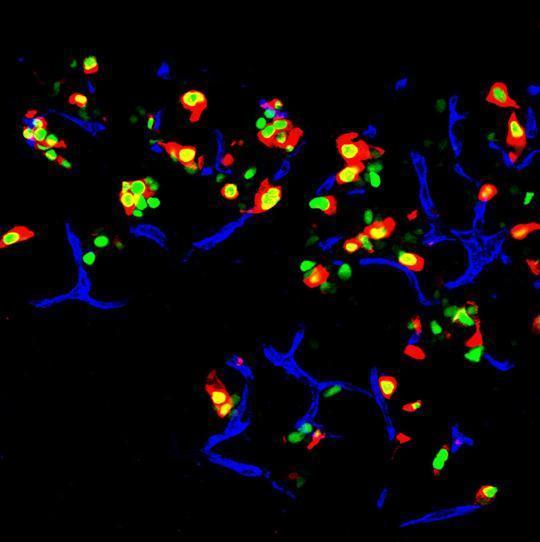
أفاد فريق ميلتون في عدد 28 أغسطس من مجلة Nature أنهم استخدموا تقنية تعرف باسم "البرمجة المباشرة" وتمكنوا من تحويل الخلايا المفرزة للهرمونات الخارجية، والتي تشكل 95٪ من خلايا البنكرياس، إلى خلايا مرموقة ونادرة. الخلية التي تنتج الأنسولين بيتا. وعندما تكون هذه الخلايا بيتا، التي تشكل واحدا بالمئة من البنكرياس، فإن الحيوان الذي يحملها يصاب بمرض السكري من النوع الأول.
وبالإضافة إلى قيمة هذا التطور بالنسبة للمجال الطبي، فإن العمل يعد خطوة للأمام نحو تطوير علاج لمرض السكري من النوع 2، وربما أخيرًا أيضًا لمرض السكري من النوع 1، وهو علاج قد يمنع حاجة المرضى إلى المراقبة. حالة السكر في الدم وتناول الأدوية أو حتى الأنسولين عن طريق الحقن. ومع ذلك، من المهم التأكيد على أنه لا تزال هناك عقبات لا حصر لها في طريق علاج البشر بناءً على هذه التجربة.
ميلتون، الباحث في معهد هوارد هيوز، قدم العمل في عدة مؤتمرات علمية في الأشهر الأخيرة وأثارت كلماته ردود فعل دهشة من المستمعين وحتى من سمعوا عنه من المستوى الثاني. وقال جورج ديلاي، الرئيس المنتهية ولايته للجمعية الدولية لأبحاث الخلايا الجذعية وعضو مجلس إدارة HSCI، إن النتائج التي توصل إليها ميلتون على نطاق "ستسبب ثورة في مجال يعد ثوريًا بالفعل".
على عكس عملية زراعة الخلايا الجذعية متعددة القدرات التي أثارت الإثارة منذ أن طرحتها قبل عامين الباحثة اليابانية شينيا ياماناكا، فإن تقنية البرمجة المباشرة هذه لا تتطلب تحويل الخلايا الناضجة إلى خلايا جذعية وعندها فقط محاولة معرفة كيفية تحويلها في الخلايا المتمايزة التي نريدها. ومع ذلك، يقول ميلتون إن طريقة إعادة البرمجة لن تلغي الحاجة إلى استخدام الخلايا الجذعية البالغة متعددة القدرات أو الخلايا الجذعية الجنينية. وقال ميلتون: "علينا أن نهاجم المشكلة من عدة زوايا"، وقال إن الأبحاث المخبرية يتم إجراؤها أيضًا على هذه الأنواع من الخلايا.
ومن الجدير بالذكر أن أحد العوائق أمام استخدام العلاج على البشر هو أن فريق ميلتون استخدم الفيروسات لإدخال العوامل المعدلة إلى الخلايا المستهدفة. ونظرًا لمخاطر هذا النهج على البشر، يبحث الفريق عن مواد كيميائية ستكون أكثر فعالية وأمانًا من الفيروسات.
للإعلان على موقع جامعة هارفارد
في نفس الموضوع:

تعليقات 2
وحقيقة أنهم تمكنوا من برمجة الخلية لم تمر مرور الكرام؟
إن الأمر أشبه باكتشاف أن السيانيد يقضي على السرطان في الفئران عن طريق الحقن المستهدف ثم الادعاء بأن هناك مشكلة في استخدام السيانيد في البشر.