أظهر الباحثون أليسون وهونجو كيف يمكن استخدام استراتيجيات مختلفة لتعطيل مكابح الجهاز المناعي في علاج السرطان. تعتبر اكتشافاتهم علامة فارقة في معركة البشرية ضد السرطان
ترجمة: د. موشيه نحماني
منحت جائزة نوبل في الطب لعام 2018 إلى اثنين من الباحثين: جيمس إليسون من الولايات المتحدة الأمريكية، وتاسوكو هونجو من اليابان. لاكتشافاتهم علاج السرطان عن طريق تثبيط التنظيم المناعي السلبي. تعتمد آلية الشفاء الخاصة بهم على مثبطات نقاط التفتيش المناعية.
ملخص
يتسبب السرطان في وفاة ملايين الأشخاص كل عام، وهو أحد أكبر التحديات التي تواجه البشرية في مجال الطب. من خلال تحفيز قدرة جهاز المناعة لدينا على مهاجمة الخلايا السرطانية، ابتكر الحائزون على جائزة نوبل في الطب لعام 2018 مفهومًا جديدًا تمامًا لعلاج السرطان.
درس جيمس إليسون بروتينًا معروفًا يعمل ككابح لجهاز المناعة. لقد فهم إمكانية إطلاق المكابح وبالتالي إطلاق خلايانا المناعية المستخدمة لمحاربة الأورام. وفي الخطوة التالية، تمكن من تطوير فكرته الجديدة إلى نهج جديد تمامًا لعلاج مرضى السرطان.
وفي الوقت نفسه، اكتشف تسوكو هونجو بروتينًا يعمل على خلايا الجهاز المناعي، وبعد اختبارات دقيقة لوظائفه، اكتشف في النهاية أنه يعمل أيضًا كمكابح لجهاز المناعة، ولكنه يعمل بمساعدة من آليات أخرى. أثبتت طرق العلاج المبنية على اكتشافه فعاليتها بشكل خاص في علاج السرطان.
أظهر الباحثون أليسون وهونجو كيف يمكن استخدام استراتيجيات مختلفة لتعطيل مكابح الجهاز المناعي في علاج السرطان. تعتبر اكتشافاتهم علامة فارقة في معركة البشرية ضد السرطان.
هل يمكن تسخير جهاز المناعة لدينا لعلاج السرطان؟
يشمل تعريف السرطان العديد من الأمراض المختلفة، والتي تتميز جميعها بالتكاثر غير المنضبط للخلايا غير الصحية التي لديها القدرة على الانتشار إلى الأعضاء والأنسجة السليمة الأخرى. تتوفر العديد من الأساليب العلاجية لعلاج السرطان، بما في ذلك الجراحة والإشعاع وأساليب أخرى، وقد أدى بعضها إلى جوائز نوبل السابقة. وتشمل هذه استخدام الهرمونات لعلاج سرطان البروستاتا (هوجينز، 1966)، والعلاج الكيميائي (إيليون وهيتشينز، 1988) وزرع نخاع العظم لعلاج سرطان الدم، وهو سرطان الدم (توماس 1990). ومع ذلك، يظل علاج السرطان المتقدم صعبًا للغاية، وهناك حاجة ماسة إلى استراتيجيات علاجية جديدة.
وفي نهاية القرن التاسع عشر وبداية القرن العشرين، ظهرت فكرة إمكانية استخدام عمل الجهاز المناعي كاستراتيجية فعالة لمحاربة الخلايا السرطانية. ونتيجة لذلك، جرت محاولات لإصابة المرضى بالبكتيريا المختلفة من أجل تنشيط نظام الدفاع. أدت هذه الجهود إلى نجاحات متواضعة بشكل خاص، ولكن يتم استخدام نسخة من هذه الطريقة حاليًا في علاج سرطان المثانة. لقد توصل المجتمع العلمي إلى استنتاج مفاده أن هناك حاجة إلى مزيد من المعرفة. بدأ العديد من العلماء في الانخراط في أبحاث أساسية واسعة النطاق في هذا المجال مع اكتشاف الآليات الأساسية التي تتحكم في جهاز المناعة، كما أظهروا كيف يمكن لجهاز المناعة التعرف على الخلايا السرطانية. على الرغم من التقدم العلمي الملحوظ، إلا أن محاولات تطوير طرق جديدة وعامة لمكافحة السرطان أثبتت أنها صعبة بشكل خاص.
مسرعات ومكابح لجهاز المناعة لدينا
السمة الأساسية لجهاز المناعة لدينا هي قدرته على التمييز بين المكونات "الذاتية" والمكونات "الغريبة" الموجودة داخل جسمنا، بحيث يكون من الممكن مهاجمة مختلف الغزاة والقضاء عليهم، مثل البكتيريا والفيروسات والآفات الأخرى. . تلعب الخلايا التائية، وهي نوع من خلايا الدم البيضاء، دورًا رئيسيًا في نظام الدفاع هذا. وقد تم اكتشاف أن هذه الخلايا التائية تحتوي على مستقبلات ترتبط بالهياكل الغريبة أثناء تنشيط جهاز المناعة. ومع ذلك، فقد وجد أن البروتينات الإضافية التي تعمل كمسرعات للخلايا التائية مطلوبة أيضًا من أجل تنشيط القوة الكاملة لجهاز المناعة (انظر الشكل). ساهم العديد من العلماء في هذا البحث الأساسي المهم وحددوا بروتينات أخرى تعمل كمكابح للخلايا التائية، مما يمنع تنشيط الجهاز المناعي. يعد هذا التوازن المعقد بين نشاط المسرعات ونشاط الفرامل ضروريًا لتحقيق التحكم الدقيق. يضمن هذا التوازن أن يعمل الجهاز المناعي بفعالية ضد الكائنات الحية الدقيقة الأجنبية مع تجنب التنشيط المفرط الذي قد يؤدي إلى تدمير مناعة الخلايا والأنسجة السليمة.
فكرة جديدة للشفاء بمساعدة جهاز المناعة
خلال التسعينيات، في مختبره بجامعة كاليفورنيا، بيركلي، قام جيمس إليسون بدراسة بروتين الخلايا التائية المسمى CTLA-4. لقد كان واحدًا من العديد من العلماء الذين أدركوا أن هذا البروتين (CTLA-4) يعمل كمكبح لنشاط الخلايا التائية. وقد استغلت فرق بحثية أخرى هذه الآلية كهدف لعلاج أمراض المناعة الذاتية. لكن أليسون كان لديها فكرة مختلفة تمامًا. في هذه المرحلة، يكون قد طور بالفعل جسمًا مضادًا يمكنه الارتباط ببروتين CTLA-4 ومنع نشاطه (انظر الشكل). قام الآن بالتحقيق فيما إذا كان نشاط CTLA-4 يمكنه فك كبح الخلايا التائية وتنشيط الجهاز المناعي حتى يتمكن من مهاجمة الخلايا السرطانية. أجرى إليسون وفريقه البحثي التجربة الأولى في نهاية عام 1994، وكانت نتائجهم مذهلة - فقد تم شفاء الفئران المصابة بالسرطان بعد علاجها بالأجسام المضادة التي تمنع الفرامل وتعيد تنشيط نشاط الخلايا التائية. على الرغم من قلة الاهتمام بهذا البحث من جانب صناعة الأدوية، واصل إليسون جهوده المكثفة لتطوير الاستراتيجية وتحويلها إلى علاج طبي بشري. بدأ نشر نتائج واعدة نيابة عن عدة مجموعات بحثية، وفي عام 2010 أنتجت دراسة سريرية مهمة نتائج واعدة بشكل خاص في المرضى الذين يعانون من سرطان الجلد المتقدم (نوع من سرطان الجلد). لدى العديد من المرضى، اختفت علامات وجود السرطان تمامًا. لم يتم رؤية مثل هذه النتائج المذهلة من قبل في هذه المجموعة من المرضى.
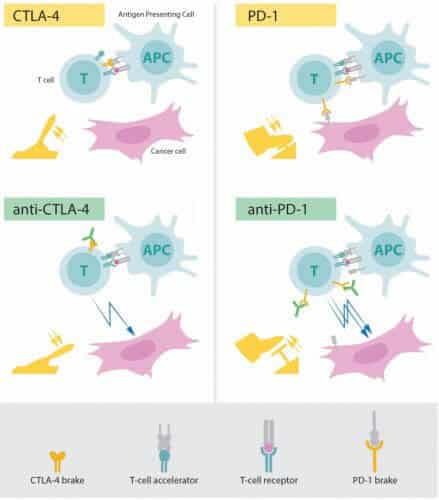
الجزء السفلي الأيسر: الأجسام المضادة (الأخضر) التي تعمل على بروتين CTLA-4 تمنع نشاط المكابح أثناء تنشيط الخلايا التائية القادرة على مهاجمة الخلايا السرطانية.
أعلى اليمين: يعمل بروتين PD-1 أيضًا كمثبط للخلايا التائية، حيث يمنع نشاط الخلايا التائية.
الجزء السفلي الأيمن: الأجسام المضادة التي تعمل على بروتين PD-1 تمنع نشاط المكابح بينما تقوم بتنشيط الخلايا التائية القادرة على مهاجمة الخلايا السرطانية.
الرسم التوضيحي: لجنة جائزة نوبل
اكتشاف البروتين PD-1 وأهميته لعلاج السرطان
في عام 1992، قبل عدة سنوات من اكتشاف إليسون، اكتشف الباحث تسوكو هونجو البروتين PD-1، وهو بروتين آخر يتم التعبير عنه على سطح الخلايا التائية. ومن أجل الكشف عن دور هذا البروتين، قام الباحث بفحص نشاطه بعناية ضمن سلسلة من التجارب الأنيقة التي أجراها على مدى سنوات طويلة في مختبره بجامعة كيوتو. وأظهرت النتائج أن بروتين PD-1، المشابه لبروتين CTLA-4، يعمل كمكابح للخلايا التائية، لكنه يعمل بآلية مختلفة. وفي إطار التجارب في BH، لوحظ أن تثبيط بروتين PD-1 يعد أيضًا استراتيجية واعدة لمكافحة السرطان، كما أثبت ذلك هونغجو ومجموعات بحثية أخرى. ومهدت هذه الاكتشافات الطريق لاستخدام هذا البروتين كهدف لعلاج مرضى السرطان. بعد التطوير السريري لهذا البروتين، أظهرت دراسة رئيسية أجريت في عام 2012 فعالية مثبتة في علاج المرضى الذين يعانون من أنواع مختلفة من السرطان. وكانت النتائج دراماتيكية، حيث لوحظ تراجع طويل الأمد وحتى شفاء كامل لدى عدد من المرضى المصابين بالسرطان المنتشر، وهي حالة كانت تعتبر في السابق غير قابلة للعلاج.
علاج السرطان اليوم وفي المستقبل بمساعدة نقاط التفتيش في جهاز المناعة
بعد الدراسات الأولية التي أثبتت النشاط المثبط للبروتينات CTLA-4 وكذلك PD-1، أصبح تطورها السريري مثيرًا. ومن المعروف الآن أن العلاج بهذا النهج، المعروف باسم "الشفاء بمساعدة نقاط تفتيش الجهاز المناعي"، قد غيّر بشكل أساسي فعالية العلاج لمجموعات معينة من المرضى المصابين بالسرطان في مراحله المتقدمة. كما هو الحال مع طرق علاج السرطان الأخرى، لوحظت هنا أيضًا آثار جانبية يمكن أن تكون خطيرة وحتى مهددة للحياة. تنجم هذه الأعراض عن الاستجابة المناعية المفرطة النشاط التي تؤدي إلى تفاعلات مناعية ذاتية، ولكن يمكن عادةً علاجها بفعالية. وتتركز الأبحاث المكثفة والمستمرة في هذا المجال حاليًا على فهم آليات النشاط، بهدف تحسين فعالية العلاجات مع تقليل الآثار الجانبية.
من بين طريقتي العلاج، ثبت أن الشفاء بمساعدة نقاط التفتيش في الجهاز المناعي باستخدام بروتين PD-1 أكثر فعالية، بعد تحقيق نتائج إيجابية في أنواع مختلفة من السرطان، بما في ذلك سرطان الرئة وسرطان الكلى وسرطان الغدد الليمفاوية وسرطان الجلد. وتشير الدراسات السريرية المحدثة إلى أن العلاج المشترك، أي تنشيط كلا البروتينين معًا، قد يكون أكثر فعالية، كما لوحظ في المرضى الذين يعانون من سرطان الجلد. وهكذا، قدم الباحثان أليسون وهونغجو الإلهام للجهود المبذولة للجمع بين الأساليب المختلفة بهدف تحرير المكابح التي تعمل على الجهاز المناعي، من أجل القضاء على الخلايا السرطانية بشكل أكثر فعالية. ويتم حاليًا إجراء عدد كبير من التجارب الطبية في إطار طرق الشفاء المعتمدة على هذا النهج ضد معظم أنواع السرطان، كما يتم اختبار وبحث بروتينات جديدة من هذه المجموعة من أجل اختبار مدى فعاليتها كأهداف لمثل هذا الشفاء.
منذ أكثر من مائة عام، حاول العلماء تسخير جهاز المناعة لمحاربة السرطان. وحتى الكشف عن الاكتشافات التي تولى المسؤولية عنها الحائزان على جائزة نوبل لعام 2018، كان التقدم في التطوير السريري لعلاج السرطان بطيئا. أدت فكرة "الشفاء بمساعدة نقاط تفتيش الجهاز المناعي" إلى طفرة في مجال علاج السرطان وغيرت بشكل أساسي طريقة علاج الأورام السرطانية.
المزيد عن الموضوع على موقع العلوم:
- جائزة نوبل في الطب لعام 2018 لمكتشفي القدرة على استخدام الجهاز المناعي لمحاربة الأورام السرطانية ومن بينهم جيمس إليسون - الحائز على جائزتي هيرفي وولف
- تم الإعلان عن الفائزين بجائزة وولف لعام 2017 في الفنون والعلوم
- سيتم منح جائزة هارفي لعام 2014 لباحث السرطان جيمس إليسون وعالم الفيزياء الفلكية راينهارد جينتزل.

تعليقات 2
بدأت زوجتي تتلقى العلاج بالدواء الجديد، بحسب الأطباء، قبل الدواء الجديد لم يكن من الممكن أن تعيش أكثر من بضعة أشهر، لقد بدأت العلاج فقط، لذلك لا توجد نتائج حتى الآن، بالمناسبة، لقد حصلت على سرطان المستوى 4 في الكلى والكبد والرئة والليمفاوية. دعونا نأمل أن يكون العلاج ناجحا. أولئك الذين يريدون المشورة، لذلك العلاج والراحة يمكن أن يتصلوا بي على الرقم 039708344 أعمل. أنا أعيش في لاس فيغاس.
كيف مر أكثر من 20 عامًا وما زالوا لا يعطوه كعلاج للأشخاص الذين هم بالفعل على حافة الموت.. حتى لو قتلهم العلاج، لقد مر عام بالفعل