طور علماء معهد وايزمان للعلوم طريقة لتسهيل إنتاج الخلايا الجذعية لدى المرضى بغرض زرعها في أجسامهم

تحمل الخلايا الجذعية الجنينية إمكانات طبية هائلة. وقد تم اتخاذ خطوة حاسمة نحو استخدامها للأغراض الطبية عندما تم اكتشاف إمكانية تخليق خلايا جذعية من الخلايا الناضجة (مثل خلايا الجلد)، وهو الاكتشاف الذي حاز على جائزة نوبل لعام 2012. إلا أن كفاءة العملية يبقى منخفضًا، ولا يتم تنسيق سلوك الخلايا. تكشف الأبحاث التي أجراها الدكتور يعقوب حنا من معهد وايزمان للعلوم، والتي نشرت مؤخرا في مجلة الطبيعة العلمية، عن المكابح التي تمنع إنتاج الخلايا الجذعية، وتزامن العملية، وتحسن كفاءتها بنسبة تصل إلى 100%. سيسهل هذا الإنجاز إنتاج الخلايا الجذعية لعلاج المرضى، كما سيعزز فهمنا للعملية الغامضة التي تتحول من خلالها خلايا الجسم الناضجة والمفرزة إلى خلايا جذعية.
أما في الخلايا الجذعية الجنينية، فإن عملية "التخصص" لم تحدث بعد، بحيث يمكنها أن تصبح أي خلية من خلايا الجسم. وبفضل هذا، يمكن استخدامها، من بين أمور أخرى، لاستعادة الأنسجة التالفة، وعلاج الأمراض التنكسية وأمراض المناعة الذاتية، وحتى زراعة الأعضاء للزراعة. ومع ذلك، فإن استخدام الخلايا الجذعية الجنينية كان محدودًا بسبب مشكلات التوافر والاعتبارات الأخلاقية. تم إحراز تقدم كبير في عام 2006، عندما اكتشف فريق من العلماء، بقيادة شينيا ياماناكا من جامعة طوكيو، أنه من الممكن "إعادة برمجة" الخلايا الناضجة وتحويلها إلى "خلايا جذعية مستحثة" (iPSC) عن طريق إدخال أربعة جينات. في نفوسهم. على الرغم من هذا الاختراق، فإن تنفيذ عملية "إعادة البرمجة" واجه صعوبات: فهي تستمر لفترة طويلة جدًا - تصل إلى أربعة أسابيع، وتحدث في الخلايا بطريقة غير متزامنة، ولا يتم سوى جزء صغير جدًا منها، أقل من خلية واحدة. بالمائة، تصبح في الواقع خلايا جذعية.
ما هو العائق - أو ما هي العوائق - التي تمنع معظم الخلايا من اجتياز عملية "إعادة البرمجة" بنجاح؟ وفي بحث ما بعد الدكتوراه، أظهر الدكتور هناء، باستخدام النماذج الرياضية، أن هذا يمثل عائقًا واحدًا على ما يبدو. ومع ذلك، فهو أول من اعترف بأنه في علم الأحياء، كما هو الحال في علم الأحياء، يجب تقديم البراهين التجريبية. وفي الدراسة الحالية، يكشف عن هوية تلك العقبة الوحيدة، ويثبت أن إزالتها تؤدي إلى تحسين فعالية "إعادة البرمجة" بشكل كبير.
وركز فريق العلماء من مجموعة الدكتورة هناء، بقيادة يواه ريس، وعساف تزفيران، وشاي غولا، والدكتورة نوا نوفيرستيرن، من قسم الوراثة الجزيئية، على بروتين معين له دور غير معروف، يسمى Mbd3. يتم التعبير عن هذا البروتين في كل خلية من خلايا الجسم، وفي جميع مراحل النمو، وهي ظاهرة نادرة، لأن العديد من البروتينات لها أدوار محددة، مما يجعلها يتم التعبير عنها في نوع معين من الخلايا، وفي مراحل التطور التي تتطلبها. اكتشف الفريق أن التعبير العام للبروتين له استثناء: فهو غير موجود في خلايا الجنين في الأيام الثلاثة الأولى من عمره، أي بعد الإخصاب مباشرة. هذه هي بالضبط الأيام الثلاثة التي تنقسم فيها الخلية الأولية المخصبة، وتنتج مجموعة من الخلايا الجذعية الجنينية متعددة الاستخدامات، والتي تتكون منها جميع خلايا الجنين. وابتداء من اليوم الرابع، تخضع هذه الخلايا للتمايز الأولي، وتفقد خاصية "تعدد الأغراض". عند هذه النقطة يأتي بروتين Mbd3 في الاعتبار.
ويبدو إذن أن غياب Mbd3 هو الذي يسمح بتكوين الخلايا الجذعية في الجنين. وقام العلماء بتقليد هذا الوضع في أنبوب اختبار، و"أعادوا برمجة" الخلايا الناضجة التي لا تنتج البروتين. النتيجة: في غضون ثمانية أيام تقريبًا، أصبحت جميع الخلايا، بطريقة متزامنة، خلايا جذعية. ويقارن الدكتور هناء الجينات الأربعة التي اكتشفها ياماناكا بـ "دواسة الوقود" التي من خلالها تبدأ عملية "إعادة البرمجة"، واكتشافه - بروتين Mbd3 - بفرامل اليد: فالسيارة تتحرك عند رفع فرملة اليد، ولكن يتعثر. يتيح خفض فرملة اليد قيادة سلسة وسريعة.
وستعمل النتائج الجديدة على تحسين طرق إنتاج الخلايا الجذعية المستحثة لعلاج المرضى بشكل كبير. وفي عملية "إعادة البرمجة" التي قام بها ياماناكا، تُستخدم الفيروسات لإدخال الجينات الأربعة في الخلايا البالغة. ولا تستخدم الطرق الطبية الفيروسات لإدخال الجينات - لأسباب تتعلق بالسلامة - كما أن معدلات نجاحها أقل من ذلك: حيث يصبح عُشر بالمائة فقط من الخلايا خلايا جذعية. تؤدي إزالة Mbd3 من الخلايا إلى تحسين كفاءة العملية وسرعتها بعدة أوامر من حيث الحجم. بالإضافة إلى ذلك، فإن اختصار مدة العملية من أربعة أسابيع إلى ثمانية أيام، وحقيقة حدوثها في جميع الخلايا في نفس الوقت، سيسمح للعلماء لأول مرة بتتبعها خطوة بخطوة، وفك رموز الآليات التي تحدث فيها. احمله. وتؤكد الدكتورة هناء أن مصدر الإنجاز هو اكتشاف المسار الطبيعي لتطور الجنين. ويقول: "إن العلماء الذين يحاولون التحقيق في عملية" إعادة البرمجة "سيستفيدون إذا حاولوا فهم كيفية تشكل الخلايا الجذعية الجنينية في الطبيعة". "فبعد كل شيء، الطبيعة هي التي تنتجها بأفضل الطرق وأكثرها كفاءة."
شارك في المؤتمر أوهاد جافني، وإيلاد تشومسكي، وسيرجي فيوكوف، ود. عبد الفتاح منصور، وعنبال كاسبي، وفلاديسلاف كروبيلنيك، وميري زاربيف، وإيتاي مازا، ونوفر مور، ودرور باران، وليهي واينبرجر من مجموعة د. هناء في قسم الوراثة الجزيئية. الدراسة؛ الدكتور إيدو أميت من قسم علم المناعة، وأعضاء مجموعته - دييغو تشيتين، ديفيد لارا إستياسو وروني بيلشر غونين؛ عاموس تاني من قسم المكافحة البيولوجية وقسم علوم الحاسوب والرياضيات التطبيقية، ومجموعته من الأعضاء زوهر شافوني ود.زوهر مشمال؛ شلوميت جلعاد والدكتورة دانييلا أمان زالزنشتاين من المركز الوطني للطب الشخصي؛ وتساحي حجاي من قسم البيولوجيا الهيكلية.
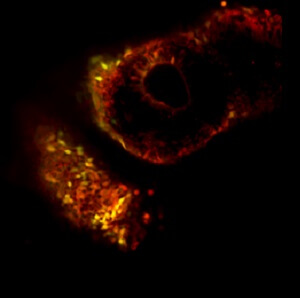
مراقبة عملية إعادة البرمجة لمدة ستة أيام. خلايا الجلد الناضجة (المميزة باللون الأحمر) التي تخضع "لإعادة البرمجة" باستخدام الطريقة التي طورها الدكتور حنا (على اليمين)، تصبح جميعها خلايا جذعية مستحثة تعبر عن علامة فلورسنت خضراء، في حين أن عددًا قليلاً فقط من الخلايا من تلك التي "تم إعادة برمجتها" وباستخدام الطريقة التقليدية (يسار) تصبح الخلايا الجذعية سباقا
كل الخيارات مفتوحة
وابتكر علماء المعهد خلايا جذعية بشرية "محايدة" تماما، والتي شكلت أنسجة داخل جنين فأر
إن إحدى العقبات الرئيسية التي تعترض طريق استخدام الخلايا الجذعية الجنينية البشرية للأغراض الطبية ترتبط على وجه التحديد بالوعد الذي تنطوي عليه هذه الخلايا: قدرتها على التمايز بسرعة إلى جميع أنواع الخلايا الموجودة. لقد بذل العلماء العديد من الجهود للحفاظ على الخلايا الجذعية الجنينية في حالتها الأولية القادرة على كل شيء، لكنها لم تنجح حتى الآن. إن البديل لاستخدام الخلايا الجذعية الجنينية ـ إنتاج الخلايا الجذعية المستحثة (iPSC) من خلال «إعادة برمجة» الخلايا البالغة ـ يعاني من نفس القيد. على الرغم من أنها يمكن أن تتمايز إلى أنواع عديدة من الخلايا، إلا أن الخلايا الجذعية المستحثة تحمل بالفعل "براعم الالتزام" إلى مسار تمايز معين. اتخذ فريق من العلماء من معهد وايزمان للعلوم مؤخرًا خطوة مهمة نحو إزالة العقبة. لقد قاموا بإنشاء خلايا جذعية بشرية "محايدة" تمامًا، أي تلك الموجودة في المرحلة الأولى من التمايز، وأبقوها على هذه الحالة لفترة طويلة. وقد يمهد هذا الإنجاز، من بين أمور أخرى، الطريق أمام إنتاج الأعضاء لزراعتها. وقد نشرت نتائج البحث مؤخرا في مجلة الطبيعة.
منذ أن تم إنتاجها بنجاح لأول مرة، في عام 2006، أصبحت الخلايا الجذعية المستحثة بديلاً أخلاقيًا ومفيدًا للخلايا الجذعية الجنينية. تتم عملية "إعادة البرمجة" عن طريق إدخال أربعة جينات في الخلايا الناضجة، مثل خلايا الجلد على سبيل المثال. بعد ذلك، يحدث نوع من "رحلة النمو إلى الوراء" في الخلايا، حتى تصل تقريبًا - ولكن ليس تمامًا - إلى حالة الخلية الجذعية الجنينية. أدرك الدكتور يعقوب حنا، من قسم الوراثة الجزيئية، وأعضاء مجموعته البحثية، طلاب البحث أوهاد جافني وليحي فاينبرجر، بالإضافة إلى علماء من المركز الوطني للطب الشخصي في معهد وايزمان للعلوم، أن إدخال نفس الشيء أربعة جينات ليست كافية "لإعادة ضبط" الخلايا؛ ويجب أيضًا إيقاف ميلهم إلى التمييز بسرعة.
إن التلميح إلى إمكانية وقف التمايز موجود في حقيقة أن الخلايا الجذعية الجنينية المشتقة من الفئران، والتي تستخدم في العديد من التجارب المعملية، تحافظ على حالتها "المحايدة"، ولا تعاني من القيود الموجودة في الخلايا الجذعية الجنينية البشرية. أدرك الدكتور حنا وأعضاء مجموعته أنهم إذا تمكنوا من فك رموز كيفية تمكن الخلايا الجذعية الجنينية للفئران من تجنب التمايز، فسيكون بمقدورهم تطبيق هذه الطريقة على الخلايا البشرية. ومن خلال مزيج من التجارب المعملية والتحليل الجيني، ابتكروا علاجًا خاصًا للخلايا الجذعية البشرية المستحثة في المختبر، مما يوقف تمايزها.
وفي وقت لاحق، قام العلماء بحقن هذه الخلايا في الخلية الأريمية - وهي جنين أولي يتكون من مجموعة من الخلايا الفردية - للفأر. إذا كانت الخلايا الجذعية البشرية المستحثة التي صنعوها محايدة تمامًا بالفعل، ويمكنها البقاء على قيد الحياة والانقسام، فسوف تتطور مع خلايا الفأر. وتم وسم الخلايا الجذعية المستحثة بصبغة الفلورسنت، مما سمح للعلماء بمتابعتها داخل جنين الفأر النامي. وأظهر الاختبار الذي تم إجراؤه بعد عشرة أيام أن هناك أنسجة مشتقة من خلايا الفأر، إلى جانب أنسجة مشتقة من الخلايا الجذعية البشرية المستحثة.
الدكتور حنا: "الخلايا التي أنشأناها تتوافق مع أقدم حالة للخلايا الجذعية الجنينية البشرية على الإطلاق. لقد تمكنا من "تجميد" عملية ديناميكية للغاية بطبيعتها، وإنتاج نوع جديد من الخلايا الجذعية المستحثة التي تكون محايدة تمامًا، وبالتالي يمكنها التمايز إلى أي نوع من الخلايا." قد يكون لهذه النتائج العديد من الاستخدامات في أبحاث الطب الحيوي، وخاصة في مجال العلاج الجيني والهندسة الوراثية. ويخطط الدكتور حنا وأعضاء فريقه لمواصلة البحث عن الأجنة المختلطة التي قاموا بإنشائها، من أجل استخدامها لاكتشاف الطرق التي من شأنها توجيه تطور الأنسجة البشرية بحيث تتشكل الأعضاء العاملة.
وفي نفس الموضوع على موقع العلوم :
لأول مرة: خلايا جذعية بشرية "محايدة" تماما، تطورت إلى أنسجة داخل جنين فأر
