إن البحث المستمر عن نقاط الضعف في فيروس الإيدز يؤدي إلى أفكار جديدة للأدوية من عائلة جديدة
بقلم غاري ستيكس، مجلة ساينتفيك أمريكان.
ظهر المقال في العدد رقم 25 من المجلة، أكتوبر-نوفمبر 2006
يستثمر الباحثون في مجال الفيروسات جزءًا كبيرًا من مواردهم في فحص كل خطوة صغيرة في دورة حياة فيروس الإيدز (HIV) - بدءًا من ارتباطه بخلية من خلايا الجهاز المناعي ودخولها إليها، وحتى تكاثرها، لإطلاق فيروسات جديدة من الخلية المضيفة والبحث عن خلية ضحية جديدة. تم تقديم آخر عائلة مهمة من الأدوية في مكافحة فيروس نقص المناعة البشرية منذ حوالي عشر سنوات مع اكتشاف مثبطات الأنزيم البروتيني. البروتياز هو إنزيم يقوم بتكسير البروتينات، وتعطل المثبطات عملها الحيوي في الخطوة الأخيرة في تكاثر الفيروس.
في ذلك الوقت، تساءل بعض أعضاء مجتمع أبحاث الإيدز عما إذا كانت مثبطات الأنزيم البروتيني يمكن أن تكون بمثابة أساس للدواء. لكن الآمال تبددت في ظل مكر الفيروس. وفي إحدى الدراسات، تم اكتشاف أن ما يصل إلى نصف حاملي الإيدز الذين يتلقون العلاج في الولايات المتحدة مصابون بفيروسات طورت مقاومة لواحد على الأقل من الأدوية التي يتناولونها. يمكن للخبراء السريريين الاختيار من بين أكثر من 20 دواءً مثبطًا للبروتياز وعائلتين من الأدوية التي تمنع الفيروس الغازي من تكرار الحمض النووي الريبوزي (RNA) الخاص به إلى الحمض النووي (DNA)، وبالتالي تخريب قدرته على التكاثر. ومن المفترض أن يؤدي إعطاء مزيج من هذه المواد ("الكوكتيل") للمرضى إلى العمل ضد القدرة الكامنة للفيروس على التحور. لكن هذا النهج لا يمنع دائمًا تطور مقاومة الأدوية، بما في ذلك مقاومة مثبطات الأنزيم البروتيني. يقول إريك فريد، الباحث في برنامج أبحاث مقاومة أدوية الإيدز في معاهد الصحة الأمريكية (NIH): "نظرًا للمقاومة المتزايدة لمثبطات الأنزيم البروتيني، فمن الأهمية بمكان إيجاد طرق جديدة لتعطيل دورة تكاثر الفيروس". .
توجد حاليًا مواد في مراحل مختلفة من التطور تتداخل مع العمليات الفيروسية داخل المضيف. تعمل هذه المواد على تعطيل العمليات في البداية أو في المنتصف أو في النهاية. يعمل الباحثون في أكاديمية وشركة صغيرة للتكنولوجيا الحيوية تدعى بانكوس في ووترتاون بولاية ماساتشوستس، مستوحاة من نجاح مثبطات الأنزيم البروتيني، لتطوير مواد جديدة، تسمى "مثبطات نضوج الفيروس"، تمنع نشاط الأنزيم البروتيني بطريقة جديدة. تهاجم مثبطات الأنزيم البروتيني بروتياز فيروس نقص المناعة البشرية بشكل مباشر، وهو هجوم يمنع الإنزيم من معالجة بروتين فيروسي يسمى GAG. عندما تخضع بروتينات GAG للقطع المناسب، فإن الأجزاء المشتقة منها تشكل قلبًا مخروطيًا، يسمى القفيصة، والذي يحيط بالحمض النووي الريبي (RNA) ويحميه. في المقابل، يقوم مثبط نضوج بانكاس بحظر موقع على بروتين GAG الذي يرتبط به البروتياز عادة. وهذا يمنع البروتياز من قطع بروتين GAG بشكل صحيح. ونتيجة لذلك، لم يتم بناء الصندوق بشكل صحيح ولا يمكن للفيروس أن يصيب خلية أخرى.
إبحث عن الأدله
بدأ الطريق إلى الدواء الذي قصده بانكوس في منتصف التسعينيات، عندما بدأت شركة بوسطن بيوميديكا بالتعاون مع أستاذ من جامعة نورث كارولينا في تشابل هيل. سعى الشركاء إلى فحص المركبات الموجودة في مجموعة من الأعشاب الطبية الصينية التقليدية بحثًا عن نشاط كيميائي حيوي ضد فيروس نقص المناعة البشرية. اكتشف مختبر كيو هسيونغ لي عقارًا مرشحًا محتملًا في عشبة طبية تايوانية.
وأظهر المركب الذي تم العثور عليه، وهو حمض البيتولينيك، نشاطا ضعيفا ضد فيروس نقص المناعة البشرية. وبعد أن قام المختبر بتحليل تركيبته الكيميائية، أصبح من الواضح أنه بعد التغيير الكيميائي يتم الحصول على مشتق له تأثير أقوى بكثير. يقول جراهام علوي، الرئيس التنفيذي للعمليات في شركة بانكوس: "كان حمض البيتولينيك نشطًا ضد فيروس نقص المناعة البشرية بتركيزات ميكرومولار". "هذا المشتق يعمل بتركيزات نانومترية."
قبل ست سنوات، قامت شركة بوسطن بيوميديكا بفصل وحدة أبحاث فيروس نقص المناعة البشرية التابعة لها وأسست شركة بانكوس، التي بدأت البحث في المركب المسمى PA-457. وهذه المرة لم تكن حالة جديدة من حالات عقار تاكسول المضاد للسرطان، والذي تطلب إنتاجه قطع أشجار الطقسوس النادرة بشكل مثير للجدل حتى تم العثور على بديل شبه اصطناعي. لم يكن بانكوس بحاجة إلى إمدادات ثابتة من الأعشاب التايوانية. يمكن استخلاص حمض البيتولينيك من أشجار الدولاف وأشجار ألبا الشائعة. أنتجت خطوة أخرى من المعالجة الكيميائية الجزيء المطلوب.
وعلى الرغم من أن الباحثين أدركوا أن PA-457 يعمل ضد جميع سلالات فيروس نقص المناعة البشرية، إلا أنه كان عليهم معرفة كيفية عمل مشتق حمض البيتولينيك ضد الفيروس على المستوى الجزيئي. أرادت الشركة فئة جديدة من الأدوية، وليس مثبطًا آخر للبروتياز. لذلك اتصلت بمختبر فريد في المعاهد الوطنية للصحة، الذي كان يدرس دورة حياة الفيروس.
وقررت مجموعة فرايد البحثية والباحثون في بانكوس أن الدواء يعمل في المراحل المتأخرة من عملية تكاثر الفيروس، ربما خلال مرحلة تكوين الصندوق. لقد عرف الباحثون بالفعل أن صندوق فيروس نقص المناعة البشرية يتشكل عندما ترتبط بروتينات GAG المشكلة حديثًا بداخل غشاء الخلية التائية المضيفة. ثم يتم تقطيعها بواسطة بروتياز فيروس نقص المناعة البشرية إلى قطع قصيرة. لقد تعلموا أيضًا أثناء عملية تطوير مثبطات الأنزيم البروتيني أن أي تعطيل في معالجة GAG من شأنه أن يجعل الفيروس غير معدٍ. ولذلك بدأوا في دراسة التفاعل بين بروتينات PA-457 وGAG، لمعرفة بالضبط كيف يعطل المركب عملية قطع GAG إلى الأجزاء اللازمة لبناء الصندوق.
زراعة المرونة
الخطوة الأولى في فهم كيفية عمل مركب معين هي في كثير من الأحيان خلق المقاومة. وهذا يسمح للعلماء بتحديد النقطة الدقيقة التي يتفاعل فيها الدواء مع موقع عمله. ولتعزيز المقاومة، قام فريد وزملاؤه بتسليم جرعة منخفضة من PA-457 إلى مزرعة الخلايا التائية المصابة بفيروس نقص المناعة البشرية. ومن ثم تم تحديد التسلسل الجيني للفيروسات المقاومة ومقارنتها بتسلسل الفيروسات التي استسلمت للدواء. يتيح هذا الاختبار تحديد موقع الموقع الذي خضع لتغيير في مقاومة الفيروسات التي تم إنشاؤها. وتبين أن هذا الموقع موجود في بروتين GAG، حيث يرتبط بالبروتياز. وقد منع هذا التغيير PA-457 من منع نشاط الإنزيم.
سمح تحليل السلالات المقاومة للباحثين بتأكيد أن PA-457 لم يعد مجرد مثبط للبروتياز. تعمل معظم الأدوية، وليس فقط مثبطات فيروس نقص المناعة البشرية، عن طريق الارتباط بالإنزيمات. يقول علوي: "إن الإجراء الموجه نحو الركيزة [بدلاً من الإنزيم] هو إجراء غير مألوف ومثير للدهشة". "ونتيجة لذلك، نعتقد أننا سنكون في وضع قوي إلى حد ما للحصول على براءة اختراع."
إن زراعة السلالات المقاومة لا يعني بالضرورة أنه من المتوقع أن يكون للدواء عمر طبي قصير. في الواقع، قد لا تتطور مقاومة PA-457 بسرعة لأن موقع الارتباط على بروتينات GAG الذي يرتبط به متشابه في سلالات مختلفة من فيروس نقص المناعة البشرية، وبالتالي لا يمكن تغييره بسهولة عن طريق الطفرات.
وقد اجتاز عقار PA-457 بالفعل مرحلة متوسطة من التجارب السريرية التي اختبرت نشاطه لدى المرضى الذين تناولوه لمدة 10 أيام مقارنة بمجموعة أخرى تناولت دواء وهميا (الدواء الوهمي). تتكاثر فيروسات الإيدز بسرعة كبيرة بحيث تكفي تجربة قصيرة لتحديد ما إذا كان الدواء يهاجم العامل الممرض في الجسم. وفي المتوسط، كان هناك انخفاض بنسبة 92% في مستوى الفيروس عند تناول أعلى جرعة وهي 200 ملليغرام. وكان هدف الدراسة هو تحقيق انخفاض بنسبة 70% على الأقل في المؤشر المسمى الحمل الفيروسي، كعلامة أولية على فعالية الدواء. إلا أن بعض المرضى لم يستجيبوا، وستحدد الشركة في مرحلة الاختبار التالية ما إذا كان من الممكن إعطاء جرعات أعلى من ذلك. يقول جيفري جاكوبسون، المسؤول عن موضوع الأمراض المعدية في كلية الطب بجامعة دريكسيل والباحث الرئيسي في التجارب السريرية: "الرسالة الرئيسية هي أن هذا دواء فعال وأن البحث يجب أن يستمر". .
وفي الجولة القادمة، سيختبر الباحثون النشاط بين الأدوية مع أدوية أخرى، وهو شرط ضروري لاختبار دواء مضاد لفيروس نقص المناعة البشرية، حيث أن علاج الإيدز يجب أن يشمل أكثر من دواء بسبب الخوف من المقاومة. في هذه الأيام، تشجع إدارة الغذاء والدواء الأمريكية (FDA) إجراء هذه الاختبارات في المراحل المبكرة من التجارب السريرية. أثناء تطوير أدوية جديدة للإيدز في الماضي، اكتشف الباحثون التفاعلات بين الأدوية والعقاقير فقط في مراحل لاحقة من عملية الاختبار السريري. وإذا سارت الأمور كما هو مخطط لها، فمن الممكن أن يسعى بانكوس إلى الحصول على موافقة إدارة الغذاء والدواء النهائية في عام 2008.
مثبطات النضج الإضافية
PA-457 ليس المثال الوحيد لمثبطات النضج، على الرغم من أنه الأكثر تقدما في السباق التجاري. وبشكل مستقل، اكتشف الباحثون في جامعة ألاباما وجامعة ميريلاند جزيئات عضوية صغيرة تمنع الوحدات الفرعية العديدة للصندوق من الاتحاد معًا لتشكل الغلاف النهائي. يقول بيتر بروفيليج، الأستاذ في قسم علم الأحياء الدقيقة بجامعة ألاباما: "نحن نحاول تغيير القطع بطريقة لا يمكن أن تتناسب مع بعضها البعض".
ويتقدم هذا النهج بالتوازي مع الأساليب الأخرى قيد التطوير المصممة لتخريب دورة حياة الفيروس. مثبطات الدخول، بما في ذلك المادة التي يبحث عنها بانكوس أيضًا، تمنع الفيروس من دخول الخلية. (أحد مثبطات الدخول، الذي يُعطى عن طريق الحقن، حصل بالفعل على موافقة إدارة الأغذية والعقاقير (FDA)، ولكن من المفترض أن يتم تناول دواء بانكوس عن طريق الفم.) ومن بين عائلات الأدوية الجديدة التي وصلت إلى مراحل متقدمة من التجارب هي مثبطات التكامل. تعمل هذه المواد على إتلاف الإنزيم الذي يسمح للحمض النووي الذي أنشأه الفيروس بالاندماج في الحمض النووي للخلية المضيفة وبالتالي منع إنتاج الحمض النووي الريبي الفيروسي الجديد. هناك حاجة إلى كل هذه العوامل البيولوجية وأكثر. وفي غياب اللقاح، الذي لا يلوح في الأفق حتى، فإن هذا الفيروس الأدنى مستوى - وهو عبارة عن كبسولة يبلغ طولها عدة نانومترات تحتوي على الحمض النووي الريبوزي المفرد - سوف يستمر في التفوق حتى على أفضل الأفكار التي يمكن لعلماء الأحياء الجزيئية أن يتوصلوا إليها.
مثبطات النضج هي عائلة جديدة من الأدوية المضادة للإيدز التي تتم دراستها حاليًا. إنهم يهاجمون الفيروس في مرحلة متأخرة من دورة حياته - عندما تتحد مكونات الفيروس التي تكونت للتو معًا لتشكل وحدات معدية جديدة تبدأ في "الصقور" خارج الخلية التائية المصابة حتى تتمكن من الاستمرار في الإصابة خلايا أخرى.
النضج الطبيعي
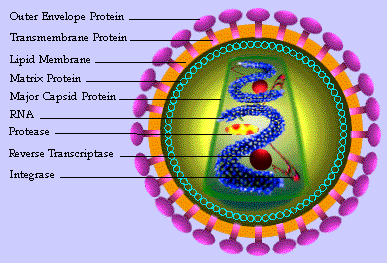
فيروس نقص المناعة البشرية
يظهر فيروس نقص المناعة البشرية (HIV) واحد كامل من خلية T مغلفة بطبقة مأخوذة من غشاء الخلية المضيفة ويتم عرض البروتينات الفيروسية على سطحها. تعمل إنزيمات البروتياز الخاصة بالفيروس على تقطيع جزيئات البروتين GAG لتكوين بروتينات أخرى أصغر.
تتحد بروتينات الصندوق لتشكل قلبًا مخروطيًا، والذي يعمل مع الصندوق النووي الداخلي على إغلاق الجينات الفيروسية الموجودة في جزيئين من الحمض النووي الريبي (RNA) المفرد الذي تقطعت به السبل ووضع الجينات الفيروسية بشكل صحيح.
الفيروس المعالج
الدواء المعين، PA-
457، يرتبط ببروتين GAG ويمنع الأنزيم البروتيني من فصل بروتين الصندوق عن البروتين المجاور في GAG - بروتين SP1.
ونتيجة لذلك، يتكون الهيكل الهجين من بروتينات الصندوق SP1 والبروتينات الصندوقية
الداخلية تأخذ شكلاً غير طبيعي. ربما يمنع هذا الفيروس من تكرار نفسه بشكل صحيح.
والمزيد حول هذا الموضوع
PA-457: مثبط قوي لفيروس نقص المناعة البشرية يعطل التكثيف الأساسي من خلال استهداف خطوة متأخرة في معالجة الكمامة. واو لي وآخرون. في وقائع الأكاديمية الوطنية للعلوم بالولايات المتحدة الأمريكية، المجلد. 100، لا. 23، الصفحات 13555-13560؛ 11 نوفمبر 2003.
انتشار مقاومة الأدوية المضادة للفيروسات القهقرية في الولايات المتحدة. دوغلاس د. ريتشمان وآخرون. في الإيدز، المجلد. 18، لا. 10، الصفحات 1393-1401؛ 2 يوليو 2004.
اكتشاف فئة من مثبطات نضوج فيروس نقص المناعة البشرية-1 الجديدة وإمكاناتها في علاج فيروس نقص المناعة البشرية. دونجلي يو وآخرون. في رأي الخبراء بشأن المخدرات التحقيقية، المجلد. 14، لا. 6، الصفحات 681-693؛ يونيو 2005.

תגובה אחת
مذهل... لكن من المستحيل حقًا العمل على لقاح حقيقي، أو ربما يكون إطلاق مثبطات جديدة باستمرار أكثر ربحية من الناحية المالية؟