باستخدام جزيئات الفلورسنت، يستطيع العلماء الآن مراقبة العلاقات المتبادلة بين الجزيئات الفردية داخل الخلايا: يمكنهم مراقبة البروتينات المشاركة في تطور الأمراض أثناء تراكمها معًا ويمكنهم مراقبة انقسام الخلايا على مستوى النانومتر.
حصل إريك بيتزيج، وويليام مورنر، وستيفان هيل على جائزة نوبل في الكيمياء لعام 2014 لمساهمتهم في التغلب على القيود العلمية المتمثلة في أن المجهر الضوئي لا يمكنه أبدًا إنتاج دقة أعلى من 0.2 ميكرومتر. باستخدام جزيئات الفلورسنت، يستطيع العلماء الآن مراقبة العلاقات المتبادلة بين الجزيئات الفردية داخل الخلايا: يمكنهم مراقبة البروتينات المشاركة في تطور الأمراض أثناء تراكمها معًا ويمكنهم مراقبة انقسام الخلايا على مستوى النانومتر.
خلايا الدم الحمراء والبكتيريا والخميرة والخلايا المنوية. عندما بدأ العلماء في القرن السابع عشر بفحص الكائنات الحية تحت المجهر الضوئي لأول مرة، انكشف أمام أعينهم عالم جديد ورائع. كانت هذه النقطة الزمنية هي ميلاد علم الأحياء الدقيقة، ومنذ ذلك الحين وحتى اليوم، أصبح المجهر الضوئي أحد أهم الأدوات في صندوق أدوات عالم الأحياء. تتطلب الطرق المجهرية الأخرى، على سبيل المثال، المجهر الإلكتروني، قياسات مدمرة على العينات التي أدت إلى موت الخلايا.
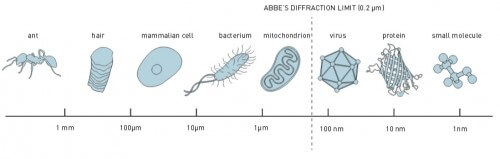
في عام 1873، نشر خبير المجهر الألماني إرنست آبي معادلة توضح كيف أن دقة المجهر محدودة، من بين أمور أخرى، بالطول الموجي للضوء. بالنسبة لمعظم علماء القرن العشرين، خلصوا بعد هذا المنشور إلى أن دقة المجهر الضوئي لن تكون أفضل من 0.2 ميكرومتر (الشكل 1). فاز الباحثون الثلاثة بجائزة هذا العام لتغلبهم على هذا القيد. وبفضل إنجازاتهم، دخل المجهر الضوئي الآن إلى عالم النانومتر. وكانت الخطوط العريضة لبعض العضيات في الخلية، على سبيل المثال، الميتوكوندريا، مرئية. ومع ذلك، لم يكن من الممكن التمييز بين الأجسام الأصغر، على سبيل المثال، لمتابعة العلاقات المتبادلة بين جزيئات البروتين الفردية داخل الخلية. إنه مشابه للموقف حيث يمكننا رؤية مباني المدينة دون أن نكون قادرين على تمييز سكان المدينة وتحركاتهم من أجل فهم وظائف الخلية بشكل صحيح وكامل، يجب أن تكون قادرًا على متابعة النشاط من الجزيئات الفردية. وعلى الرغم من أن المعادلة التي وضعها آبي صحيحة وموجودة، إلا أنه تم العثور على طرق للتحايل عليها. قام الفائزون بجائزة نوبل في الكيمياء لعام 2014، إريك باتزيج، وويليام مورنر، وستيفان هيل، بإدخال المجهر الضوئي إلى بُعد جديد، وهو البعد النانومتري، بمساعدة جزيئات الفلورسنت. ومن الناحية النظرية، لم يعد هناك أي هيكل أصغر من أن يتم فحصه. ونتيجة لذلك، أصبح الفحص المجهري هو الفحص النانوي.
قصة التغلب على قيود آبي تتحرك على محورين منفصلين - تم منح الفوز لمبدأين منفصلين تم تطويرهما بشكل مستقل عن بعضهما البعض. تبدأ القصة في عام 1993 في شقة طلابية في جنوب غرب فنلندا، عندما جاء ستيفان هيل بفكرة رائعة أثناء تصفح كتاب مدرسي عن البصريات الكمومية.
تمرد الشباب على حد احتمال آبي
حاول ستيفان إيجاد طريقة للالتفاف حول القيود التي وضعها إرنست آبي قبل أكثر من قرن من الزمان. كانت الرغبة في تحدي مثل هذا المبدأ الراسخ مغرية في نظر ستيفان. إلا أن كبار العلماء في ألمانيا سكبوا الماء البارد على حماسته فهرب شمالاً إلى مكان أكثر برودة. عرض عليه أستاذ في جامعة توركو كان يعمل في مجال الفحص المجهري الفلوري منصبًا في فريقه البحثي. كان هيل مقتنعاً بضرورة وجود طريقة للتغلب على حد الاحتمال الذي وضعه آبي، وعندما قرأ مصطلح الانبعاث القسري في كتاب عن البصريات الكمومية، طرأت على ذهنه فكرة جديدة في عام 2009.
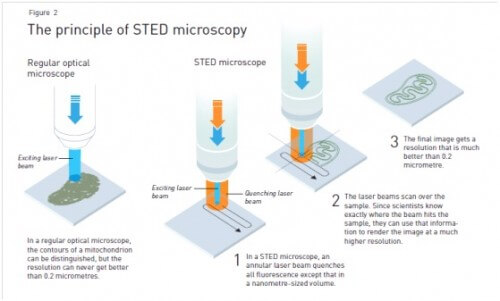
الحل الذي توصل إليه هو: "مصباح يدوي" نانومتري يقوم بمسح العينة
وفي مختبره الجديد، عمل ستيفان في مجال الفحص المجهري الفلوري، وهي طريقة يستخدم فيها العلماء جزيئات الفلورسنت لتصوير أجزاء من الخلية. على سبيل المثال، يمكنهم استخدام الأجسام المضادة الفلورية التي ترتبط بشكل انتقائي بالحمض النووي الخلوي. يقوم العلماء بتحفيز الأجسام المضادة إلكترونيًا بومضة قصيرة من الضوء، مما يجعلها تتوهج في غمضة عين. إذا كانت الأجسام المضادة مرتبطة بالحمض النووي، فسوف تكون حذرة من مركز الخلية، حيث يتم ضغط الحمض النووي في نواة الخلية. وبهذه الطريقة، يستطيع العلماء معرفة الموقع الدقيق للجزيء. ومع ذلك، في هذه المرحلة لم يتمكن العلماء إلا من وضع مجموعات من الجزيئات، مثل خيوط الحمض النووي المتشابكة. كانت الدقة منخفضة جدًا للتمييز بين خيوط الحمض النووي المنفصلة - حاول أن تتخيل أنك قادر على رؤية ملف من الخيوط دون رؤية الخيوط المنفصلة نفسها. عندما قرأ ستيفان عن الانبعاث القسري، أدرك أنه يمكن إنتاج نوع من مصباح يدوي نانومتري يمكنه مسح العينة، نانومترًا تلو الآخر. من خلال استخدام الانبعاث القسري، يتمكن العلماء من إخماد فلورة الجزيئات، حيث يقومون بتوجيه شعاع الليزر نحو الجزيئات التي تفقد طاقتها على الفور وتتحول إلى اللون الأسود. في عام 1994 نشر ستيفن هيل مقالاً يشرح أفكاره بالتفصيل. في الطريقة المقترحة، والتي تسمى استنفاد الانبعاث المحفز (STED)، يثير وميض الضوء جميع جزيئات الفلورسنت، في حين يثبط وميض آخر من الضوء الفلورة من جميع الجزيئات باستثناء تلك التي يبلغ حجمها نانومتر (الشكل 2). وفي الخطوة التالية، يتم امتصاص هذه الجزيئات فقط. ومن خلال مسح العينة وقياس مستويات الضوء بشكل مستمر، يمكنك الحصول على صورة شاملة ومفصلة. كلما كان حجم الفلورسنت الذي ينبعث منه أصغر في لحظة معينة، زادت دقة الصورة النهائية. لذلك، ومن حيث المبدأ، لم يعد هناك أي حد لدقة المجاهر الضوئية.
تطوير أول مصباح يدوي نانومتري لـ ستيفان هيل في ألمانيا
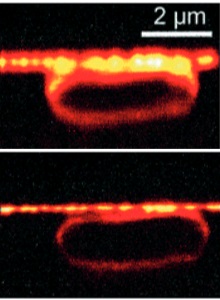
لم تسبب ورقته النظرية أي ضجة فورية، ولكن كان من المثير للاهتمام أن عُرض عليه منصب في معهد ماكس بلانك للكيمياء الفيزيائية الحيوية في غوتنغن. وفي السنوات التالية، وضع أفكاره موضع التنفيذ وطوّر مجهرًا يعمل وفقًا لمبدأ STED. وفي عام 2000، كان قادرًا على إثبات أن أفكاره تعمل فعليًا كما هو متوقع بطريقة عملية، وذلك من بين أمور أخرى، من خلال إجراء تصوير لبكتيريا الإشريكية القولونية بقدرة فصل لم يتم تحقيقها من قبل بمساعدة المجهر الضوئي (الشكل 3). XNUMX).
وعلى النقيض من هذه الطريقة، فإن المبدأ الثاني الذي فاز به العلماء، وهو الفحص المجهري لجزيء واحد، يتضمن استخدام صور متعددة، واحدة فوق الأخرى. ساهم كل من ويليام مورنر وإريك بيتزيج بشكل مستقل برؤى أساسية مختلفة لتطوير هذه الطريقة. تم وضع الأساس عندما تمكن مورنر من تحديد موقع جزيء فلورسنت صغير واحد.
ويليام مورنر - أول من حدد موقع جزيء فلورسنت واحد
في معظم الطرق الكيميائية، على سبيل المثال أثناء قياس الامتصاص أو التألق، يقوم العلماء بفحص ملايين الجزيئات في وقت واحد. تمثل نتائج هذه الأنواع من التجارب نوعًا من الجزيء النموذجي المتوسط. وكان على العلماء أن يتقبلوا هذه الحقيقة، حيث لم تكن هناك أداة أخرى، لكنهم ظلوا يحلمون بقياس جزيء واحد. وذلك في ضوء حقيقة أنه كلما كانت التفاصيل أكثر وأكثر ثراءً، كلما كان من الممكن فهم العمليات البيولوجية بشكل أفضل، على سبيل المثال - تطور المرض.
وهكذا، عندما أصبح مورنر في عام 1989 أول عالم على الإطلاق يقيس امتصاص الضوء لجزيء واحد، كان ذلك إنجازًا رائدًا. في تلك المرحلة كان يعمل في مركز أبحاث IBM. في سان خوسيه، كاليفورنيا. مهدت تجربته الطريق لمستقبل جديد وألهمت العديد من الكيميائيين الآخرين لتحويل انتباههم إلى الجزيئات المنفردة. وكان أحد هؤلاء العلماء إريك باتزج، الذي سنعرض إنجازاته أدناه.
وبعد ثماني سنوات، اتخذ مورنر الخطوة التالية نحو الفحص المجهري لجزيء واحد، معتمدًا على الاكتشاف الذي أكسب مخترعه جائزة نوبل - البروتين الفلوري الأخضر (GFP).
يتم تشغيل وإيقاف المصابيح الكهربائية الجزيئية
وفي عام 1997، انضم مورنر إلى جامعة كاليفورنيا، سان دييغو، حيث كان روجر تيسيان، الحائز على جائزة نوبل في المستقبل، يحاول جعل بروتين الفلورسنت الأخضر يتوهج بجميع ألوان قوس قزح. وتم عزل البروتين الأخضر من قنديل البحر المتألق وتكمن أهميته في قدرته على جعل بروتينات أخرى داخل الخلايا الحية مرئية بوضوح. وباستخدام تقنيات الجينات، يربط العلماء البروتين الفلوري الأخضر ببروتينات أخرى. في الخطوة التالية، يكشف الضوء الأخضر عن مكان وجود البروتين المسمى بالضبط في الخلية.
اكتشف مورنر أن فلورة إحدى سلالات البروتين الفلوري الأخضر يمكن إيقاف تشغيلها وتشغيلها بناءً على رغبة الباحث. وعندما أثار البروتين بالضوء عند طول موجي 488 نانومتر، بدأ البروتين يتوهج، ولكن بعد فترة بدأ التوهج في التلاشي. وبغض النظر عن كمية الضوء التي وجهها الباحث إلى البروتين، فإن التألق يتلاشى تدريجياً حتى يختفي. ومع ذلك، فقد تبين أن الضوء ذو الطول الموجي 405 نانومتر قادر على إحياء البروتين. عندما تم إعادة تنشيط البروتين، عاد إلى التألق عند طول موجة 488 نانومتر.
قام مورنر بنقع هذه البروتينات في هلام، ووضعها بحيث تكون المسافة بينها أكبر من عتبة آبي البالغة 0.2 ميكرومتر. ونظرًا لأنها كانت موزعة بشكل متناثر، يمكن للمجهر الضوئي العادي التمييز بين وميض كل بروتين على حدة - فهي تعمل مثل المصابيح الكهربائية الصغيرة مع مفاتيح التشغيل والإيقاف. ونشرت النتائج في عام 1997 في مجلة الطبيعة المرموقة.
وبهذا الاكتشاف أثبت مورنر أنه يمكن التحكم بصريًا في فلورة الجزيئات المفردة. لقد حلت فكرة مورنر المشكلة التي صاغها إريك باتزج قبل عامين.
لقد استنفدت الأكاديمية - لكنني ما زلت ملتزمًا بشأن حدود احتمالية آبي
تمامًا مثل ستيفان هيل، كان إريك بيتزج مهووسًا بالتغلب على حد احتمالات والده. وفي أوائل التسعينيات، عمل على مجهر ضوئي جديد يسمى مجهر المجال القريب، في مختبرات بيل في نيوجيرسي. في الفحص المجهري للمجال القريب، يتم تسليط شعاع الضوء من طرف صغير للغاية يقع على بعد بضعة نانومترات فقط فوق العينة. يمكن لطريقة الفحص المجهري هذه أيضًا التغلب على قيود آبي، ولكنها تحتوي أيضًا على نقاط ضعف كبيرة. على سبيل المثال، الضوء المسقط له نطاق قصير جدًا بحيث يصعب رؤية الهياكل الموجودة أسفل سطح الخلية.
في عام 1995، توصل إريك باتزج إلى أن هذا الفحص المجهري لا يمكن تحسينه بشكل أكبر. بالإضافة إلى ذلك، لم يشعر بالارتياح في الأوساط الأكاديمية وقرر إنهاء مسيرته البحثية؛ ودون أن يعرف إلى أين يتجه من هناك، تقاعد من شركة Bell Labs. ومع ذلك، ظل حد الاحتمال الذي وضعه آبي يزعجه. أثناء المشي في يوم شتاء بارد، خطرت في ذهنه فكرة جديدة: هل من الممكن التغلب على حد التضخيم باستخدام جزيئات ذات خصائص مختلفة، جزيئات ذات فلورة بألوان مختلفة؟
استلهامًا من بحث مورنر، من بين علماء آخرين، كان إريك باتزج قادرًا بالفعل على اكتشاف التألق في جزيء واحد باستخدام المجهر القريب من المجال. بدأ يتساءل عما إذا كان المجهر العادي يمكنه إنتاج قوة فصل عالية كهذه إذا توهجت جزيئات مختلفة بألوان مختلفة، على سبيل المثال - الأحمر والأصفر والأخضر. وكانت الفكرة التي تبادرت إلى ذهنه هي أن المجهر سيسجل صورة واحدة لكل موضوع. إذا كانت جميع الجزيئات من نفس اللون متناثرة وتقع على مسافة تتجاوز حد آبي وهو 0.2 ميكرومتر، فيمكن تحديد موقعها بدقة كبيرة. في الخطوة التالية، عندما يتم وضع هذه الصور المنفصلة واحدة فوق الأخرى، ستؤدي الصورة الإجمالية إلى ظهور قوة فصل ستكون أفضل بكثير من قدرة أبا، وسيكون من المستحيل تمييز الجزيئات ذات الألوان المختلفة حتى لو كانت مختلفة. تفصل بينهما عدة نانومترات. ومع ذلك، كان هناك عدد من المشاكل العملية، على سبيل المثال، عدم وجود جزيئات ذات كمية كافية من الخصائص البصرية المميزة.
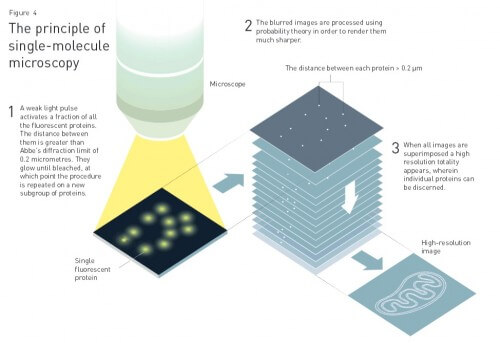
في عام 1995، نشر إريك بيتزج أفكاره النظرية في المجلة العلمية Optics Letters، وبعد ذلك تقاعد من المجال الأكاديمي وانضم إلى شركة والده التجارية.
إغراء العودة إلى الفحص المجهري بعد اكتشافات بروتينات الفلورسنت الخضراء
لسنوات عديدة، كان إريك باتزيج معزولًا تمامًا عن مجتمع الأبحاث. ومع ذلك، في أحد الأيام المشرقة، عاد شغفه بالعلم إلى الحياة مرة أخرى، وأثناء قراءته للأدبيات العلمية، صادف البروتين الفلوري الأخضر لأول مرة. بعد أن أدرك أن هناك بروتينًا قادرًا على ظهور بروتينات أخرى داخل الخلايا، بدأ باتزج في طرح الفكرة في ذهنه والتي يمكنه من خلالها التغلب على قيود آبي. وجاء الإنجاز الحقيقي في عام 2005 عندما عثر على بروتينات فلورية يمكن للباحث تفعيلها، على غرار تلك التي اكتشفها مورنر في عام 1997 على مستوى جزيء واحد. أدرك بيتزيج أن مثل هذا البروتين هو الأداة التي يحتاجها لتنفيذ الفكرة التي توصل إليها قبل 10 سنوات. ليس من الضروري أن تكون لجزيئات الفلورسنت ألوان مختلفة، يمكنها ببساطة أن تتوهج في أوقات مختلفة.
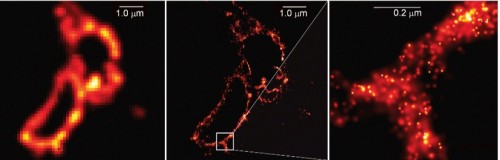
التغلب على قيود آبي من خلال تكديس الصور
وبعد مرور عام واحد فقط، أثبت إريك بيتزيج، بالتعاون مع العلماء الذين عملوا على إثارة البروتينات الفلورية، أن فكرته نجحت في الممارسة العملية. ومن بين تجاربهم الأخرى، ربط العلماء البروتين المضيء بالغشاء المحيط بالليزوسوم، وهو محطة دورة الخلية. وبمساعدة وميض من الضوء، تم تنشيط البروتينات وأصبحت متألقة، ولكن نظرًا لأن الوميض كان ضعيفًا للغاية، بدأ بعضها فقط في التوهج. نظرًا لعددها الصغير، تم العثور على جميع البروتينات تقريبًا على مسافة أكبر من حد اكتشاف آبي وهو 0.2 ميكرومتر. وبخلاف ذلك، يمكن تسجيل الموقع الدقيق لكل بروتين تحت المجهر. وبعد فترة، يتلاشى التألق ثم يقوم العلماء بتنشيط مجموعة فرعية جديدة من البروتينات. ومرة أخرى، كان الوميض ضعيفًا جدًا لدرجة أن بعض البروتينات فقط بدأت في التوهج، ثم تم تسجيل صورة أخرى لها. وعندما قام بيتزج بجمع الصور واحدة فوق الأخرى، انتهى به الأمر إلى الحصول على صورة فائقة الدقة للغشاء الليزوزومي. كان مستواها أفضل من حد احتمالية والدها. في نهاية المطاف، قدمت مقالة نشرت في المجلة العلمية المرموقة Science في عام 2006 هذا العمل الرائد.
لا يزال الفائزون يرسمون خرائط لأعمق أسرار الحياة
وأدت الأساليب التي طورها الباحثون الثلاثة إلى تطوير العديد من الأساليب النانوية المستخدمة اليوم في جميع أنحاء العالم. ولا يزال الفائزون الثلاثة باحثين نشطين في المجتمع العلمي المتنامي للباحثين في مجال الفحص النانوي. وعندما يوجهون مناظيرهم النانوية القوية نحو أصغر مكونات الحياة، فإنهم يزودوننا أيضًا بالمعرفة الأكثر تقدمًا في نفس الوقت. قام ستيفان هيل بالتنقيب داخل الخلايا العصبية الحية من أجل فهم أفضل للمشابك العصبية في الدماغ. درس مورنر البروتينات المرتبطة بمرض هنتنغتون. تابع إريك باتزج انقسام الخلايا داخل الأجنة. هذه مجرد جزء صغير من العديد من الأمثلة. هناك شيء واحد مؤكد - الفائزون بجائزة نوبل في الكيمياء لعام 2014 وضعوا الأسس لتطوير المعرفة ذات الأهمية الكبرى للجنس البشري.

تعليقات 10
إريك بيتزيج لا أعتقد ذلك
اليوم، استخدام مجاهر المجال الساطع والمجاهر المظلمة في المجال المرئي يجعل من الممكن أيضًا مراقبة الهياكل النانوية باستخدام المجهر الضوئي. يتعلق الأمر بانكسار وانعكاس أشعة الضوء، وتكون الأجسام النانومترية مرئية بوضوح (نرى أسلاك Si-nano بسهولة). وهذا التأثير معروف منذ أكثر من 15-20 عامًا.
والأكثر روعة، العلم في أفضل حالاته.
تبدو بعض الرسوم التوضيحية مثل المجرات
إلبينتزو
فهمت. أنا مهتم لماذا المجهر هو الكيمياء، والذين تعاملوا مع المواد الكيميائية حصلوا على جائزة في الفيزياء...
لم يكن هذا هو القصد. عندما كتبت الرد كان العنوان "نوبل للفيزياء 2014:...". لقد تم تغييرها منذ ذلك الحين إلى الكيمياء والآن كل شيء على ما يرام.
إلبينتزو
"مايكرو" صغير، و "نانو" قزم. في الواقع ليس اسما سيئا ...
العنوان غير صحيح.