وقد يؤدي هذا الاكتشاف إلى تطوير علاجات مستهدفة لشفاء إصابات الجهاز العصبي المحيطي، وربما في المستقبل حتى في الجهاز العصبي المركزي.
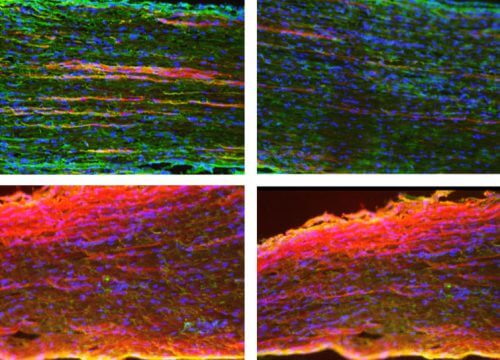
إعادة نمو امتدادات الخلايا العصبية المحاطة بالخلايا الدبقية (نواة الخلية محددة باللون الأزرق)، في العصب الوركي للفأر، بعد سبعة أيام من الإصابة (أعلى) وبعد 25 يومًا من الإصابة (أسفل). في الفئران التي لا تحتوي على Silc1 (العمود الأيسر)، تكون عملية الاستعادة أقل قوة - تكون امتدادات الخلايا العصبية المعاد نموها (الحمراء) أقصر منها في الفئران التي تحتوي على نسخة نشطة من Silc1. تم تصويرها باستخدام المجهر الفلوري
تعمل الجينات التي تشفر البروتينات في الغالب في وقت واحد في أنسجة مختلفة وفي مواقف مختلفة، وبالتالي فإن زيادة نشاطها أو تقليله قد يعالج مرضًا في عضو واحد، ولكنه يسبب آثارًا جانبية غير مرغوب فيها في الأعضاء الأخرى. في المقابل، فإن الجينات التي لا ترمز للبروتينات ولكن يتم نسخها إلى جزيئات تحكم، تسمى جزيئات الحمض النووي الريبي الطويلة غير المشفرة (RNA الطويلة غير المشفرة) أو lncRNA للاختصار، لها تخصص ضيق - يتم التعبير عنها في أنسجة محددة وتحت ظروف جيدة. -ظروف محددة. حدد علماء معهد وايزمان للعلوم مؤخرًا جين lncRNA الذي يلعب دورًا حاسمًا في إصلاح الخلايا العصبية. وهذا الاكتشاف، الذي ورد في المجلة العلمية Molecular Cell، قد يؤدي إلى تطوير علاجات مستهدفة لشفاء الإصابات في الجهاز العصبي المحيطي، وربما في المستقبل حتى في الجهاز العصبي المركزي.
ولأن جينات lncRNA لا ترمز للبروتينات، فقد تجاهلها العلماء لسنوات عديدة. فقط في العقد الماضي تم اكتشاف هذه الجينات كعوامل تحكم مهمة للجينوم. على سبيل المثال، تشارك في التحكم في تكوين الخلايا وانقسامها أثناء نمو الجنين وأيضًا في الجسم البالغ. يقول رئيس المجموعة البحثية الدكتور إيجور أوليتسكي من جامعة هارفارد: "يوجد أكثر من 20 ألف جين من جينات lncRNA في الجينوم البشري - ربما أكثر من جينات ترميز البروتين - لكننا حتى الآن لم نكتشف دور سوى حفنة قليلة". قسم المكافحة البيولوجية.
قام الدكتور أوليتسكي وأعضاء مجموعته - الدكتور راتم بن طوف بيري، وهاداس هزروني، وميكا غولدريتش - بالتحقيق في أدوار lncRNA في الجهاز العصبي المحيطي للثدييات، حيث يتم التعبير عن مجموعة واسعة بشكل خاص من هذه الجينات غير المشفرة. عندما تتضرر الخلايا العصبية في اليدين والقدمين وبقية الجهاز العصبي المحيطي، فإنها تعيد نمو امتداداتها، وهذا على عكس الجهاز العصبي المركزي، أي الدماغ والحبل الشوكي. إن سبب هذا السلوك المختلف للخلايا العصبية في كل نظام ليس واضحًا، خاصة في ضوء حقيقة أن كلاهما لديه آليات نمو مماثلة أثناء التطور الجنيني. اختبر الدكتور أوليتسكي وزملاؤه ما إذا كانت الـlncRNAs قد تساهم في حل هذا اللغز.
إن الشفاء الذاتي للخلايا العصبية في الجهاز العصبي المحيطي ليس مثاليًا ويستغرق وقتًا طويلاً. ومن الممكن في المستقبل أن يكون من الممكن تطوير علاجات من شأنها تسريع عملية الشفاء".
من اليمين: د. إيغور أوليتسكي، ميخا غولدريتش، د. راتم بن طوف بيري. "التخصص الضيق"
ولتحقيق هذه الغاية، أجرى العلماء خريطة جينية للفئران المصابة بإصابة في العصب الوركي. ووجدوا أنه بعد حوالي أسبوع من الإصابة، عندما بدأ العصب في التجدد، قفز التعبير عن نوع معين من lncRNA عشرة أضعاف. واكتشف العلماء أيضًا أن هذا الجين -الذي أطلقوا عليه اسم Silc1- يبدأ برنامجًا شفاءيًا يتم من خلاله تنشيط جين قريب، والمعروف أنه يلعب دورًا في إعادة نمو الخلايا العصبية فقط.
أجرى العلماء بعد ذلك سلسلة من التجارب التي أثبتت الدور المركزي لـ Silc1 في إعادة نمو الخلايا العصبية: عندما زادوا التعبير عن Silc1 في الخلايا العصبية في المزرعة، زاد النمو بنسبة 40% مقارنة بالخلايا العصبية الطبيعية؛ في المقابل، عندما منع العلماء التعبير عن Silc1 في الفئران المعدلة وراثيا، كان تجديد العصب الوركي التالف أقل كفاءة وأبطأ من الفئران غير المعدلة وراثيا. يتم التعبير عن أهمية Silc1 أيضًا من خلال حقيقة أنه أحد جزيئات lncRNA النادرة نسبيًا - في المجمل، هناك حوالي 1,000 منها - والتي تم الحفاظ عليها طوال التطور وتوجد في جميع الثدييات، بما في ذلك الفئران والجرذان والبشر.
وأظهرت تجارب أخرى أن Silc1 لديه "تخصص ضيق" بشكل خاص: فهو يظهر فقط في كائن حي ناضج، فقط بعد إصابة الخلايا العصبية المحيطية - وفقط في تلك التي تغطيها طبقة المايلين الواقية. قد يسمح هذا التخصص بتطوير علاجات تستهدف الخلايا العصبية التالفة والتي لن تسبب آثارًا جانبية في الأنسجة الأخرى. "إن الشفاء الذاتي للخلايا العصبية في الجهاز العصبي المحيطي ليس مثالياً ويستغرق وقتاً طويلاً - على سبيل المثال، فترة إعادة التأهيل بعد إصابة العصب الوركي، وهو أوسع وأطول عصب (يبلغ طوله حوالي 100 سم) في الإنسان الجسم، قد يستمر لمدة عام كامل،" كما يقول د.ر. أوليتسكي. "من الممكن في المستقبل أن يكون من الممكن تطوير علاجات من شأنها تسريع عملية الشفاء." وقد يفتح اكتشاف الجين أيضًا اتجاهًا جديدًا للبحث نحو إمكانية علاج الأضرار التي لحقت بالجهاز العصبي المركزي. في هذه الدراسات، سيكون من الضروري التحقق مما إذا كان تعبير Silc1، أو أي إجراء يحاكي هذا التعبير، يمكن أن يساعد الخلايا العصبية التالفة، على سبيل المثال في الحبل الشوكي، على إعادة النمو.
