أعاد الباحثون في معهد أبحاث الملاريا بجامعة جونز هوبكنز هندسة بكتيريا موجودة في أمعاء بعوضة الأنوفيلة، مما جعلها تنتج سموم تقتل طفيليات الملاريا الموجودة في البعوض، لكنها لم تضر البعوض أو البشر. ووفقا للدراسة، التي نشرت العام الماضي في المجلة العلمية المرموقة PNAS، تمكنت البكتيريا المعدلة وراثيا من "شفاء" جزء كبير من البعوض الذي شارك في الدراسة، وإزالة طفيليات الملاريا من أمعائها.
ومن الصعب أن نفكر في مرض يضر البشرية أكثر من الملاريا. ويتعرض نصف سكان العالم لخطر الإصابة بهذا المرض القاسي الذي يسبب نوبات من الحمى الشديدة والحمى والإرهاق. ويصاب ما بين 300 إلى 500 مليون شخص بالمرض مرة أخرى كل عام، وذلك بشكل رئيسي نتيجة للدغات البعوض. ومن بين المصابين، يموت أكثر من مليون شخص بسبب المرض كل عام، وهو رقم يعادل 3,000 شخص كل يوم. ومن سخرية القدر أن الملاريا تؤثر بشكل أساسي على الدول النامية في آسيا وأفريقيا، مما يزيد من شل اقتصاد هذه الدول، وقدرة مواطنيها على تحقيق العيش الكريم.
كيف تنتقل الملاريا من شخص لآخر؟ على عكس أمراض مثل الجدري أو الأنفلونزا، التي تنتقل عبر الهواء، فإن طفيليات الملاريا حساسة وحساسة للمخاطر البيئية. إنهم بحاجة إلى المساعدة للانتشار من شخص لآخر. ومن حسن حظهم أن الله الطيب -بمساعدة التطور- صمم لهم أداة مثالية: بعوضة الأنوفيلة.
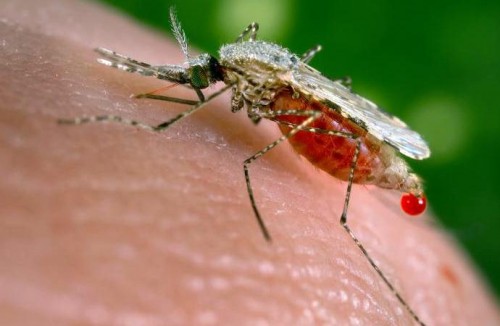
في المرة الأولى التي رأيت فيها أحد بعوض الأنوفيلة، لم يبدو الأمر مختلفًا عن البعوض المزعج المعتاد في الرحلات الميدانية المدرسية السنوية: جناحان وستة أرجل وإبرة واحدة. لكن بعوضة الأنوفيلة تحمل سرها الخبيث في أمعائها وغددها اللعابية. عندما تذهب أنثى البعوض للصيد، فإنها تركز بشكل خاص على البشر العصير وتمتص دمائهم بشهوة كبيرة. وكجزء من عملية المص، تقوم بإدخال "الحداك" - وهي حقنة صغيرة توضع على وجهها - في الجلد وتمتص الدم. ولمنع تخثر الدم أثناء الشفط، تحقن البعوضة في الجرح لعاباً يحتوي على مضادات التخثر... وأيضاً طفيليات الملاريا الموجودة في أمعائها وغددها اللعابية.
تستعد البعوضة لمص الدماء بشكل مرضي. في الأصل من ويكيبيديا.
تستعد البعوضة لمص الدماء بشكل مرضي. في الأصل من ويكيبيديا.
ماذا نستطيع ان نفعل؟ وقد باءت المحاولات المتكررة لاستخدام المبيدات الحشرية ضد البعوض بالفشل، لأنها تمر بتطور سريع وتتكيف مع بعض السموم. وقد باءت محاولة تطوير لقاح فعال ضد الملاريا بالفشل في الوقت الحالي لسبب مماثل: حيث تتأقلم الطفيليات بشكل جيد مع جهاز المناعة البشري، وتتكيف معه بسرعة.
ولكن ماذا لو استخدمنا الهندسة الوراثية، ووجهنا كل قوى الطبيعة ضد طفيليات الملاريا؟
فكرة استخدام الهندسة الوراثية كوسيلة للتعامل مع الملاريا موجودة منذ سنوات عديدة، لكنها في الماضي كانت تتعلق بشكل أساسي بإعادة هندسة البعوض نفسه. ففي نهاية المطاف، إذا كانت الطفيليات تحتاج إلى البعوض للانتقال من شخص لآخر، فما علينا سوى تعديل البعوض ليكون مقاومًا للطفيليات. ولكن من السهل التحدث، ومن الصعب القيام به. إن الهندسة الوراثية لأي كائن حي ليست لعبة أطفال، والمخلوقات المعقدة مثل البعوض تتطلب عملاً شاقاً من جانب الباحثين في المختبرات. علاوة على ذلك، يواجه البعوض المعدل وراثيًا صعوبة في التزاوج مع البعوض "الطبيعي"، وبالتالي سيواجه أيضًا صعوبة في الازدهار في البرية.
لقد فهم مارسيلو جاكوبس لورنا، الباحث في جامعة جونز هوبكنز، الطبيعة الإشكالية للهندسة الوراثية للبعوض، وقرر التركيز على كائن حي آخر: البكتيريا التي تعيش في أمعاء البعوض. تعيش هذه البكتيريا في نفس العضو الذي تنمو فيه طفيليات الملاريا أيضًا، وتتكاثر بشكل كبير فور مص البعوضة للدم، وتزداد أعدادها مئات وآلاف المرات. باختصار، إنها المرشحة المثالية لاستهداف طفيليات الملاريا، لحظة وصولها إلى أمعاء البعوض.
مثل هذه الفكرة الجيدة لا تبقى يتيمة، وقد تم بالفعل إجراء العديد من الدراسات في هذا المجال. قبل 16 عامًا، كانت هناك محاولة للتعامل مع مرض شاغاس، الذي ينتقل عن طريق الخنافس، عن طريق هندسة بكتيريا موجودة أيضًا في جسم الخنفساء. عملت جاكوبس لورنا نفسها سابقًا على هندسة البكتيريا ضد الملاريا، وقبل ست سنوات نجحت في إعادة هندسة بكتيريا الإشريكية القولونية، بحيث تقدم جزيئات على غلافها الخارجي تضعف قدرة طفيليات الملاريا على النمو والنضج في البعوض و الفئران.
تمكنت هذه التطورات المبكرة من إثبات قيمة الفكرة، لكن بكتيريا الإشريكية القولونية المهندسة لا توجد عادة في أمعاء البعوض، وبالتالي لم تكن قادرة على البقاء هناك أيضًا. القلة التي نجت واجهت مشكلة أخرى: الجزيئات القاتلة التي أنتجتها لم يتم إطلاقها في الأمعاء وأثرت على جميع الطفيليات، لكنها ظلت قريبة من البكتيريا، وبالتالي كانت قدرتها محدودة على قتل طفيليات الملاريا.
في منتصف عام 2012، نجحت جاكوبس لورنا في إعادة هندسة البكتيريا التي تعيش بشكل طبيعي في أمعاء البعوض، والتي تستجيب للاسم اللاتيني لكسارة الأسنان Pantoea agglomerans. لقد أدخلت فيها آلية مشابهة لتلك الموجودة في الإشريكية القولونية، لكنها غيرتها بحيث يتم إطلاق البروتينات القاتلة هذه المرة في السوائل المعوية، بدلا من البقاء ملتصقة بالبكتيريا. وكان أملها هو أن تتمكن البكتيريا الجديدة من البقاء على قيد الحياة بشكل جيد في الأمعاء، وتقتل طفيليات الملاريا. وقد تحقق هذا الأمل بالكامل. أكل البعوض البكتيريا مع الماء المحلى بالسكر الذي تلقاه، وتمكنت الميكروبات الصغيرة من البقاء والنمو داخل البعوض، مما أدى إلى إطلاق جزيئات قتل الطفيليات في تجويف الأمعاء.
النتائج؟ ومن بين مجموعة البعوض التي لم تتلق العلاج بالبكتيريا المعدلة وراثيا، بقي نحو تسعين في المئة من الحشرات مصابة بطفيليات الملاريا. ومن بين المجموعة التي تلقت البكتيريا المعدلة وراثيا، بقي 14 في المائة فقط مصابين - أي انخفاض بأكثر من خمسة وسبعين في المائة في عدد حاملات البعوض.
وتحمل هذه النتائج أنباء مشجعة فيما يتعلق بمستقبل مكافحة الملاريا. في المستقبل المنظور، سنكون قادرين على إطلاق الأمراض المعدية التي ستفيدنا نحن البشر. سنقوم بإصابة البعوض بالبكتيريا باستخدام مرافق تغذية خاصة تحتوي على ماء سكر وميكروبات. وكل بعوضة تتاح لها الفرصة لتلقي البكتيريا هي بعوضة لن تنقل العدوى إلى شخص أو شخصين أو عشرة أشخاص بالملاريا.
وبطبيعة الحال، لا يزال الطريق طويلا نحو مثل هذا المستقبل. هناك أكثر من مائة نوع مختلف من بعوض الأنوفيلة قادر على حمل طفيليات الملاريا، وقد يتفاعل كل منها بشكل مختلف مع البكتيريا. ويجب على المرء أيضًا أن يدرس بعناية وجدية العواقب المترتبة على إطلاق البكتيريا المعدلة وراثيًا في الطبيعة، والتحقق مما إذا كانت قد لا تسبب ضررًا بيئيًا أو تنقل الجينات إلى بكتيريا أخرى وتمنحها قدرات غير عادية.
وعلى الرغم من كل هذه القيود، وجميع العقبات التي لا تزال في الطريق، فإن المستقبل يبدو واعدا. تزودنا الهندسة الوراثية الآن بالأسلحة الأساسية الحقيقية في مكافحة الملاريا. لن يتم بعد الآن تغطية أطفال وأحفاد الإنسانية بالناموسيات. سيتعين على طفيليات الملاريا، التي تسبب مرضا يرافق الإنسان منذ أكثر من عشرة آلاف سنة، أن تتعامل مع البكتيريا التي ينتجها الإنسان في العقود المقبلة.
حان وقت الانتقام.

تعليقات 5
ادعم صاحب التعليق أعلاه. كل هذا العبث يخلق، على مستوى النسبة المئوية، عتبة عالية جدًا لتكاثر الأميبات داخل مجموعة بكتيرية صحية ولتنظيم الأستروبالتوجين في حالة من الجمود البركاني الصغير. يتم تدمير حوالي سبعين بالمائة من جميع الجراثيم في مثل هذه العملية، ولا داعي للقلق من عدم إمكانية التطعيم ضد الملاريا بهذا القدر.
مثل هذه التجربة خطيرة والفشل فيها يمكن أن يكون كارثيا
من المستحسن التفكير بعناية قبل الاستخدام
يدعم أسلافي
يوم جيد
سابدارمش يهودا
ادعم التعليق أعلاه،
في أستراليا، حاولوا القضاء على الأنبون بمرض الورم المخاطي الذي قضى عليهم بنسبة 100٪ تقريبًا، وبالطبع بعد بضعة أجيال، شكلت القلة التي نجت من السكان مجموعة سكانية جديدة ومحصنة.
إذا كانت طفيليات الملاريا قد طورت مقاومة للقاحات في جسم الإنسان، فلماذا لا تطور أيضًا مقاومة ضد الجزيئات القاتلة لنباتات Pantoea agglomerans؟ نجا 14% => ليس بعدة أجيال حتى أكلت مجموعة طفيليات الملاريا بأكملها نباتات Pantoea agglomerans على الإفطار
إنني ذكي، ويستحق الاستثمار من جانب الحكومات المتقدمة، وأحلم باليوم الذي نستطيع فيه تطبيق نفس المبادئ على داء الكلب، وأنفلونزا الطيور، وما إلى ذلك.