قام الباحثون في التخنيون بتطوير تقنية مبتكرة لتخصيص دواء مضاد للسرطان ليناسب المريض. وفي هذه العملية التي تشبه اختبار الحساسية، يتم اختبار كميات ضئيلة من الأدوية المختلفة داخل الورم السرطاني في جسم المريض. وأشرف على البحث البروفيسور آفي شرودر من كلية الهندسة الكيميائية.
قام الباحثون في التخنيون بتطوير تقنية تشخيصية جديدة للاختبار المبكر لمدى ملاءمة الدواء المضاد للسرطان لمريض معين، حتى قبل بدء سلسلة العلاجات. البحث، الذي نُشر في مجلة Nature Communications، ترأسه البروفيسور المشارك آفي شرودر من كلية الهندسة الكيميائية في التخنيون. تم تمويل البحث من خلال منحة ERC-H2020 المرموقة من الاتحاد الأوروبي وكذلك من المؤسسة الوطنية للعلوم.
وجمعية السرطان.
يوضح البروفيسور شرودر: "إن عالم الطب يتجه حاليًا نحو الطب الشخصي". وهذا تغيير نموذجي ناتج عن التطور الهائل في فهم الجينوم البشري وفهم أن الأشخاص المختلفين يتفاعلون بطرق مختلفة لنفس المعاملة. ومع ذلك، حتى العلاجات المتوافقة مع الخصائص الجينية للمريض لا تقدم في بعض الأحيان الصورة الكاملة عن المريض، عند اختيار الدواء المناسب. في الواقع، يتلقى العديد من المرضى دواءً لا يستجيب له السرطان. هذه هي خلفية بحثنا الذي قمنا في إطاره بتطوير تقنية تتغلب على هذه العقبة".
قام البروفيسور شرودر وطالب الدكتوراه تسفي ياري وباحثون آخرون في فريق البحث بتطوير مختبر صغير (وآمن) يختبر فعالية الدواء المحدد في جسم مريض معين. "إنه يذكرنا إلى حد ما باختبارات الحساسية، التي تزودنا باختبار بسيط لملف الحساسية الخاص بشخص معين. نحن هنا نتحدث عن اختبار بسيط يوفر، بالمثل، ملف استجابة المريض للدواء المقصود. هذه الطريقة تجعل من الممكن فحص فعالية عدة أدوية في نفس الوقت داخل الورم السرطاني للمريض، بجرعات قليلة والتي لا يشعر بها المريض ولا تعرضه للخطر على الإطلاق. وبناء على هذا الاختبار، سيتم اختيار الدواء الأكثر فعالية للمريض المحدد."
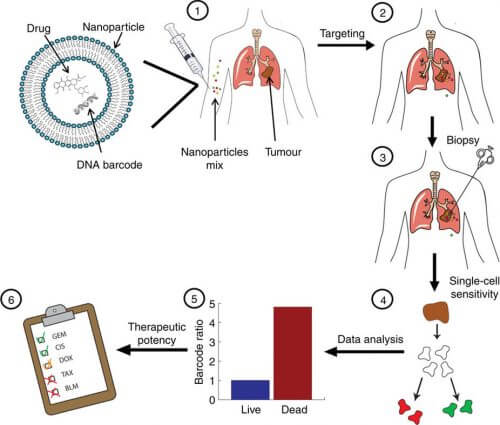
كيف تفعل ذلك؟ "نحن نعبئ كميات صغيرة من الأدوية المضادة للسرطان داخل جزيئات نانوية مخصصة قمنا بتطويرها. ما يميز هذه الحزم النانومترية هو أنها تتدفق في الدورة الدموية إلى الورم حيث تبتلعها الخلايا السرطانية. ونقوم بإرفاق تسلسل الحمض النووي الاصطناعي بهذه العبوات مسبقًا، والتي تعمل بمثابة قارئات الباركود لنشاط الدواء في الخلايا السرطانية."
وبعد 48 ساعة، يتم أخذ عينة (خزعة) من الورم، ويقدم تحليل الباركود معلومات دقيقة عن الخلايا التي تم تدميرها (أو لم يتم تدميرها) بواسطة كل دواء. "وبعبارة أخرى، يراقب هذا النظام تأثير كل دواء على الخلايا السرطانية للمريض. في الوقت الحالي، نعمل مع أدوية مسجلة كمضادات للسرطان، ولكن من حيث المبدأ من الممكن اختبار مجموعة من الأدوية لكل مريض وبالتالي معرفة الدواء الأكثر ملاءمة له للمرض الذي يعاني منه".

ركزت الدراسة الحالية، التي استندت إلى تجارب على الفئران، على تأثير الأدوية المختلفة على سرطان الثدي الثلاثي السلبي، وهو نوع من السرطان يمثل تحديًا خاصًا، ولا يستجيب بشكل جيد للعلاجات القياسية ويجعل من الصعب على الأطباء مطابقة الدواء. للمريض. للتأكد من أن التجربة تختبر بالفعل تأثير الدواء نفسه، وليس تأثيرًا محتملاً لحالة النانومتر نفسها، تم أيضًا إدخال "حزم دواء وهمي" فارغة من الدواء في الأورام. النتيجة: تم العثور على الأدوية المضادة للسرطان في نهاية العملية بشكل رئيسي في الخلايا السرطانية الميتة - أي أنها قتلتها - بينما تم العثور على عبوات الدواء الوهمي بشكل رئيسي في الخلايا الحية للورم، أي أنها لم تدمرها الخلايا. عند مقارنة الأدوية المضادة للسرطان المختلفة، تم العثور على اختلافات أيضًا في فعالية الأدوية المختلفة.
يقول البروفيسور شرودر: "تعطي هذه التكنولوجيا نافذة جديدة لرؤى أساسية حول آليات السرطان ومقاومته للأدوية المختلفة، لكن فكرتي قابلة للتطبيق أيضًا: كيف يمكن لأبحاثنا أن تساعد الناس. ولذلك فإن النجاح الحالي سعيد ومثير للغاية. صحيح أن الأمر يتطلب الكثير من العمل لجعل تطويرنا منتجًا متاحًا للجمهور، لكنني أعتقد أننا سنراه في العيادات في غضون سنوات قليلة.
البروفيسور شرودر هو عضو هيئة التدريس في كلية التخنيون للهندسة الكيميائية وعضو في معهد راسل بيري لتكنولوجيا النانو (RBNI) ومركز أبحاث السرطان المتكامل في التخنيون (TICC). في السنوات الأخيرة، أصبح البروفيسور شرودر أحد أبرز رواد الأعمال العلميين في مجال التكنولوجيا الحيوية الإسرائيلية، وشكلت أبحاثه في التخنيون الأساس لتأسيس العديد من الشركات، بما في ذلك شركة ViAqua Therapeutics، التي تطور لقاحات لتربية الأحياء المائية؛ InPlant Technologies - شركة تعمل على تحسين جودة البيئة وكفاءة وسلامة الرش في الزراعة الدقيقة؛ PEEL Therapeutics - شركة أمريكية تعمل على تطوير أدوية مبتكرة لعلاج السرطان، استنادًا إلى نظام التحكم داخل الخلايا P53 الفريد الموجود في الأفيال؛ وشركة Moebius Medical، التي طورت علاجًا مبتكرًا لمرض التهاب المفاصل التنكسي. تم تسجيل التكنولوجيا المبتكرة التي تم تطويرها كبراءة اختراع، وهناك مفاوضات حاليًا لتسويقها مع صندوق رأس المال الاستثماري NGT3.
وقالت الرئيسة التنفيذية لجمعية السرطان، ميري زيف: “نحن فخورون بالمساهمة في مثل هذه الدراسة المهمة والواعدة التي قد توفر استجابة شخصية للمرضى وتؤدي إلى علاج أكثر كفاءة ودقة. لدينا علاقة ممتازة طويلة الأمد مع التخنيون بشأن هذه القضايا. كما استفاد البروفيسور أهارون تشاشانوفر، الحائز على جائزة نوبل في الكيمياء لعام 2004، من المنح البحثية التي تقدمها الجمعية في بداية حياته المهنية كباحث شاب. وقد عمل البروفيسور تشاشانوفر طوعًا كعضو في لجنة الأبحاث التابعة للجمعية لمدة عقد من الزمن، ويشغل حاليًا منصب رئيسنا الفخري."
