وعلى غرار "البصمات" الجينية التي تستخدمها الشرطة في حربها ضد الجريمة، فإن فك رموز الحمض النووي للأورام الخبيثة سيساعد العلماء في حربهم ضد السرطان.

وعلى غرار "البصمات" الجينية التي تستخدمها الشرطة في حربها ضد الجريمة، فإن فك رموز الحمض النووي للأورام الخبيثة سيساعد العلماء في حربهم ضد السرطان. تكمن إحدى أكبر العقبات في حقيقة أنه ليس مجرمًا واحدًا: فهناك ما لا يقل عن 200 نوع من السرطان، والعديد من الأنواع الفرعية. الهدف هو فك رموز "بصمات الأصابع" لكل نوع من الأنواع المختلفة، بحيث يتلقى مرضى السرطان في نهاية المطاف علاجات شخصية.
تم تحقيق تقدم مهم نحو هذا الهدف مؤخرًا من خلال التعاون بين معهد وايزمان للعلوم والمعهد العريض بجامعة هارفارد ومعهد ماساتشوستس للتكنولوجيا. يؤدي طرفا هذا التعاون إلى مختبر البروفيسور إيتان دوماني، في قسم فيزياء الأنظمة المعقدة في معهد وايزمان: منذ حوالي ثلاث سنوات، تلميذه السابق، الدكتور جاد جيتز، مدير قسم التحليل الحسابي حاليًا لجينوم السرطان في معهد برود، بدأ العمل بالتعاون مع الدكتور القس يوتام دراير، وهو طالب أبحاث (في ذلك الوقت) للبروفيسور دوماني في المعهد.

الجينوم السرطاني هو تجميع الحمض النووي للخلية الخبيثة. ويتميز كل نوع من السرطان بوجود عيوب معينة في الجينوم. وتشارك مجموعة الدكتور جيتز في معهد برود، والتي تضم نحو 30 عالما في الأحياء والكيمياء الحيوية والفيزياء ومهندسي البرمجيات، في مشروع "أطلس جينوم السرطان" الذي تديره المعاهد الوطنية الأمريكية للصحة، وفي مشاريع أخرى تهدف إلى نفس الهدف: فك رموز الجينومات لجميع أنواع السرطان الرئيسية.
أصبحت هذه المشاريع الطموحة ممكنة بفضل التكنولوجيا المبتكرة التي تم تطويرها منذ بضع سنوات، وهي التسلسل عالي الإنتاجية، والذي يسمح "بقراءة" العديد من أجزاء الحمض النووي في نفس الوقت. فقد أدى ذلك إلى تسارع كبير في عملية تسلسل الحمض النووي، وأيضا إلى انخفاض كبير بنفس القدر في تكلفته: من 30 ألف دولار في عام 1999 مقابل مليون "حرف" من الحمض النووي، إلى 10 سنتات في عام 2011. ونتيجة لذلك، أصبح بإمكان العلماء الآن إجراء التسلسل بسرعة مئات من جينومات الأورام السرطانية، يحتوي كل منها على مليارات من أزواج قواعد الحمض النووي. لكن تسلسل الحمض النووي ليس كافيا: فليس أقل صعوبة أن نفهم ما يكمن في هذا الطوفان من المعلومات الجينومية.
تعمل مجموعة الدكتور جيتز في معهد برود على تطوير أدوات حسابية لتحليل هذه المعلومات. أثناء زيارته لمعهد وايزمان في ديسمبر 2008، سأل جيتز دوماني، مشرفه السابق، عما إذا كان أي من طلابه الحاليين مهتمًا بالمشاركة في هذا البحث. أوصى دوماني يوتام دراير. حقيقة أن جيتز ودراير ينحدران من خلفيات مماثلة - كلاهما خدم في جيش الدفاع الإسرائيلي كجزء من "تالفيوت"، حيث حصل كلاهما على شهادات جامعية في الرياضيات والعلوم الدقيقة الأخرى (جيتز في الفيزياء، ودراير في علوم الكمبيوتر) - ضمنت تعاونًا مثمرًا .
هذا ما حدث. طور دراير خوارزمية تسمى BreakPointer، والتي تقوم بمسح الجينوم البشري بأكمله وتجد السمات المميزة للسرطان: عيوب في إصلاح الحمض النووي تؤدي إلى تغييرات هيكلية تختلف عن تسلسل الحمض النووي الطبيعي. وكانت هذه هي الخوارزمية الأولى التي تمكنت من تحديد نقاط التوقف الدقيقة في الحمض النووي حيث تحدث التبادلات. يقول الدكتور جيتز: "أصبحت هذه الأداة الآن جزءًا مهمًا لا يتجزأ من جهودنا لرسم خريطة لجميع الجينات وجميع الظواهر التي تساهم في الإصابة بالسرطان".
لقد تم دمج BreakPointer في جميع تحليلات جينوم السرطان في معهد برود، وقد ساعد بالفعل في عدد من الاكتشافات العلمية الهامة، بما في ذلك اكتشاف الاضطرابات التي سمي عليها: نقاط التوقف التي تؤدي إلى تبادل الحمض النووي. وكما ورد في مجلة Nature، ساعد BreakPointer في اكتشاف نمط غير معروف سابقًا من تبادلات الكروموسوم في سرطان البروستاتا: سلاسل معقدة من التبادلات داخل جينات السرطان أو بالقرب منها. علاوة على ذلك، اكتشف العلماء علاقة بين موقع نقاط التوقف وحالة الكروماتين، وهو مكون مهم في العبوة الواقية للكروموسومات، مما يشير إلى أن التبادلات الجينية قد تكون مرتبطة ليس فقط بالجينات،
ولكن أيضًا للعوامل اللاجينية، أي تلك التي لم يتم تشفيرها بشكل مباشر في الجينوم.
وفي دراسة عن سرطان القولون، نشرت في مجلة Nature Genetics، اكتشف العلماء الذين يستخدمون الخوارزمية 11 عملية تبادل للحمض النووي أدت إلى انضمام الجينات بشكل غير طبيعي. وكان من بينها الجين "التسلسلي"، الذي يظهر في عدد كبير من الأورام المختلفة - وتم اكتشاف الجين الأول من هذا النوع في سرطان القولون. الجينات المرتبطة بطريقة غير طبيعية تنتج بروتينات غير طبيعية، وهذه يمكن أن تكون هدفا للعلاجات المستهدفة في المستقبل، ليس فقط لأنها ضرورية لوجود السرطان، ولكن أيضا لأنها غير موجودة في الخلايا السليمة، وبالتالي فإن يمكن أن يركز العلاج على الخلايا السرطانية دون الإضرار بالأنسجة السليمة.
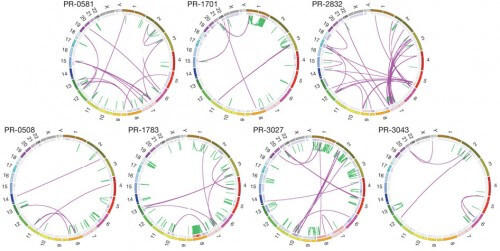
يقول الدكتور دراير، وهو حاليًا باحث ما بعد الدكتوراه في كلية الطب بجامعة هارفارد وباحث ما بعد الدكتوراه في كلية الطب بجامعة هارفارد: "يحدد BreakPointer الموقع الدقيق لفواصل الحمض النووي عن طريق تحديد موقع التسلسلات المشبوهة في الجينوم السرطاني، ومقارنتها بالمناطق المقابلة في الجينوم الطبيعي". معهد واسع. "بمساعدة الخوارزمية، وجدنا اتصالات محتملة بين تبادلات الحمض النووي وغيرها من خصائص الجينوم، مثل الطفرات أو حالة الكروماتين." تم وصف هذه العلاقات وأهميتها البيولوجية في أنواع مختلفة من السرطان مؤخرًا في المجلة العلمية Genome Research.
إن رسم خرائط جميع الجينومات السرطانية الرئيسية سيسمح للعلماء بفهم أفضل للعمليات الجزيئية التي تسبب السرطان، وبالتالي تعزيز تطوير الأدوية التي تتكيف مع العيوب الجينية الفريدة لكل ورم. توجد بالفعل علاجات مستهدفة من هذا النوع لعدة أنواع من السرطان، ويتزايد عددها باستمرار. في المستقبل، سيقوم الأطباء بشكل روتيني برسم خريطة للجينومات لجميع مرضى السرطان، بهدف تصميم علاج شخصي وفعال وآمن لكل منهم.
