شركة Ogmedics، التي تأسست قبل عام وفازت بالمركز الأول في مسابقة "BizTech" في التخنيون، جمعت 3 ملايين شيكل من حاضنة TerraLab في Kneam * ReWalk تطلق الجيل السادس من الهيكل الخارجي
حاضنة TerraLab، التي تعمل كجزء من برنامج حاضنة كبير العلماء، تستثمر 3 ملايين شيكل في شركة Augmedics LTD - وهي شركة تأسست كجزء من مسابقة BizTech في التخنيون، وفازت بالمركز الأول في BizTech 2014.
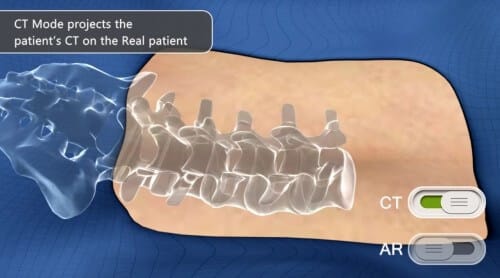
يساعد النظام الذي تطوره شركة Augmedics - ARGUS - الجراحين على تحسين مستوى الجراحة وسلامتها. أثناء العملية، يرتدي الجراح نظارات الواقع المعزز، والتي تعرض كائنات محاكاة ثلاثية الأبعاد على المريض. على سبيل المثال، في جراحة العظام، يقدم النظام للجراح، في الوقت الفعلي، صورة لعظام المريض في موضعها الفعلي ويسمح له بإجراء الجراحة بدقة، كما لو كان يرى العظام من خلال الجلد. ويظهر النظام في الفيديو التالي:
ومع فوز أوغميديكس بالمسابقة العام الماضي، قال الرئيس التنفيذي للشركة، نيسان إليميليتش، إن "المسابقة زودتنا بأدوات عملية لصياغة خطة العمل وبمساعدة عملية من الموجهين، وقبل كل شيء أعطتنا إطار عمل وأدخلتنا إلى روتين العمل. كل هذا ساعدنا في تطوير التكنولوجيا وتخطيط التوجهات المستقبلية في تطوير منتجنا ARGUS."
في الأسبوع الماضي، تم اختيار المتأهلين للتصفيات النهائية لنهائيات BizTech 2015. ومن بين 85 فريقًا قدم ترشيحات للمسابقة، تم اختيار 12 فريقًا، بما في ذلك Renty - منصة إقراض المعدات المدفوعة التي تربط بين المقرضين والباحثين؛ Genees - روبوتات متعددة الاستخدامات تعتمد على Arduino ويمكن التحكم فيها من الهاتف الذكي؛ LabSuit - نظام مبتكر لإدارة المخزون وبيع المواد للمختبرات في مجال الكيمياء والأحياء. وInfuse - حل قائم على البرمجيات (فقط) للتنقل داخل المباني.
تطلق ReWalk الجيل السادس من الهيكل الخارجي - للاستخدام في المنزل وفي المجتمع
تطلق الشركة الإسرائيلية ReWalk Robotics، الشركة المصنعة لأنظمة الهياكل الخارجية الآلية، أحدث إصدار من النظام الشخصي، ReWalk Personal 6.0. يقدم الجيل السادس من النظام لضحايا النخاع الشوكي منتجًا مطورًا، والذي يوفر، من بين المزايا الأخرى، أعلى سرعة للمشي والتكيف الأكثر دقة للمستخدم. هذا هو الإصدار الأحدث من نظام ReWalk، الذي حصل على موافقة إدارة الأغذية والعقاقير (FDA)، وهو مخصص للاستخدام في المنزل وفي المجتمع.
وقال لاري جاسينسكي، الرئيس التنفيذي لشركة ReWalk: "إن إطلاق الإصدار 6.0 يمنح مرضى إصابات النخاع الشوكي هيكلًا خارجيًا، مصممًا ليناسب المستخدم بشكل أفضل، مما يسمح بالمشي بشكل أسرع وتحسين التحكم في المشي مقارنة بالجيل السابق". "تعتمد جهود التخطيط لدينا على سنوات عديدة من الاستخدام من قبل مستخدمي النظام وفلسفة تدعو إلى تحسين المنتج، بحيث يناسب جميع جوانب الحياة اليومية. يوفر التصميم التخصيص على أعلى مستوى من خلال برنامج يسمح بتعديل القياسات والتشريح لكل مستخدم على حدة. كل ذلك يعمل على تحسين تجربة المستخدم مقارنة بالإصدارات السابقة ومقارنتها بأنظمة الهيكل الخارجي الأخرى، والتي تخضع للتجارب السريرية حول العالم."
تشمل مزايا نظام ReWalk 6.0 ما يلي: تعديل دقيق للغاية - لقياسات المستخدم وإنتاجه وفقًا للمواصفات الشخصية، مما يسمح بتحسين الوظيفة والسلامة والتوازن بين مفاصل المستخدم. سرعة مشي أعلى - أظهرت الدراسات السريرية التي أجريت باستخدام جهاز ReWalk أن مستخدمي النظام قادرون على المشي بسرعة 0.71 متر في الثانية، وهو أسرع من أي نظام هيكلي خارجي آخر. تصميم أكثر كفاءة - تؤدي إزالة المجموعة الخلفية إلى تقليل الوزن الواقع على الكتفين وتمنح المستخدم حرية اختيار الملابس والحركة. يتيح التصميم الجديد والنظيف للأشرطة والأسطح المبطنة للمستخدم ارتداء النظام وإزالته بسهولة أكبر وبسرعة محسنة.
وقالت جودي: "إن الخبرة التي اكتسبناها في الاستخدام اليومي لأنظمة ReWalk والتعليقات التي نتلقاها من المجتمع، بالإضافة إلى التقدم التقني الذي حققه فريق البحث والتطوير لدينا، جعلت من الممكن تطوير وتصنيع الجيل التالي من الهيكل الخارجي الاصطناعي". جيريكي، مدير التسويق والتدريب لشركة ReWalk. "تُظهر تعليقات المستخدمين على الإصدار 6.0 أنهم يتمتعون بملاءمة أفضل وتحكم أفضل في الخطوات ومزيد من الراحة، وذلك بفضل إزالة المجموعة الخلفية في النموذج المحسن."
ReWalk هي الشركة المصنعة الوحيدة للهياكل الخارجية في الولايات المتحدة الأمريكية التي حصلت على موافقة إدارة الأغذية والعقاقير (FDA) لكل من النظام الشخصي (الشخصي) ونظام إعادة التأهيل (إعادة التأهيل) للمنتج. وحصلت الشركة أيضًا على موافقة الجهات التنظيمية للأنظمة التي تقوم بتصنيعها في مناطق أخرى من العالم، بما في ذلك أمريكا الشمالية وأوروبا وآسيا والشرق الأوسط وأستراليا. يعد ReWalk هو الهيكل الخارجي الأكثر استخدامًا على نطاق واسع حول العالم، مع أنظمة للاستخدام الشخصي وأنظمة للاستخدام في مراكز إعادة التأهيل في العديد من البلدان.
تقدم مجموعة HBL Hadassit Bio تقارير عن الموافقات على براءات الاختراع لشركة Selcure التابعة
حصلت شركة Selcure Neurosciences الإسرائيلية من مجموعة HBL للبورصة والمملوكة لشركة Hadassit Bio بنسبة 21.2%، على موافقة لتسجيل براءة اختراع في الولايات المتحدة الأمريكية بعنوان: طرق زراعة الخلايا الجذعية الجنينية والتمايز المتحكم فيه. براءة الاختراع مملوكة لشركة ES Cell International، التي منحت Selcure ترخيصًا حصريًا لاستخدام براءة الاختراع. تشير براءة الاختراع إلى طرق توجيه تمايز الخلايا الجذعية الجنينية ونضوجها إلى خلايا سلفية وهي مهمة في حماية تقنية Selcure لإنشاء خلايا ناضجة مثل الخلايا العصبية للزرع والتجديد.
منتج Selkiur's OpRegen مخصص لعلاج مرض تنكس الشبكية Dry AMD، الذي يحتوي على خلايا صبغية (RPE) لشبكية العين مستخرجة من الخلايا الجذعية الجنينية من أصل بشري باستخدام طريقة تمايز الخلايا الحاصلة على براءة اختراع. حصلت شركة Selcure على موافقات إدارة الغذاء والدواء ووزارة الصحة لبدء التجارب السريرية لمنتج OpRegen بالإضافة إلى موافقة لجنة هلسنكي في مركز الأبحاث السريرية في مركز هداسا الطبي في القدس لإجراء التجارب السريرية 1 و 2
يعلن كامادا عن نشره في المجلة العلمية Pediatric Diabetes
أعلنت شركة Kamada، وهي شركة أدوية تنتج منتجات تعتمد على بروتينات البلازما وتركز على الأدوية اليتيمة، عن نشر بيانات إيجابية في المجلة المتخصصة لمرض السكري لدى الأطفال من المرحلة 1/2 من التجربة السريرية لمنتجها الرائد، alpha-1 antitrypsin (AAT) من أصل بشري يمكن إعطاؤه عن طريق التسريب لعلاج الأطفال المصابين بداء السكري من النوع الأول (T1D) الذين تم تشخيصهم حديثًا.
في دراسة المرحلة 1/2 ذات العلامة المفتوحة التي استمرت 37 أسبوعًا، تم اختبار الأطفال المصابين حديثًا بداء السكري من النوع الأول (T1D). شملت الدراسة 1 مريضًا تلقوا 24 علاجًا بجرعة 18 أو 40 أو 60 ملغم/كغم/جرعة من AAT على مدى 80 أسبوعًا. وكانت المؤشرات الرئيسية في التجربة هي السلامة والتحمل. وشملت التدابير الثانوية السيطرة على نسبة السكر في الدم، والببتيد C، ومستويات الأجسام المضادة. تم تعريف المستجيبين المحتملين للعلاج على أنهم مرضى لديهم مستويات الببتيد C التي أظهرت انخفاضًا بنسبة أقل من 28٪ عن خط الأساس.
لم يتم الإبلاغ عن أي آثار جانبية كبيرة، أو حالات الحماض الكيتوني (DKA)، أو حالات نقص السكر في الدم الشديدة. لم تكن الآثار الجانبية مرتبطة بالجرعة وكانت عابرة. تحسنت التدابير المتعلقة بتوازن نسبة السكر في الدم أثناء الدراسة في جميع المجموعات، بغض النظر عن الجرعة. انخفض الهيموجلوبين السكري (HbA1c) من 8.43% إلى 7.09% (المتوسط، p <0.001). في نهاية الدراسة، كان لدى 18 شخصًا (75٪) قيم ذروة الببتيد C ≥0.2 بمول / مل، وتم اعتبار ثمانية مرضى (33.3٪) مستجيبين محتملين وتميزوا بفترة أقصر من مرض السكري لدى الأحداث عند الدخول. التجربة (54.5 ± 34.3 مقابل 95.9 ± 45.7 يومًا، p = 0.036) وانخفاض أكبر في مستويات HbA1c خلال فترة الدراسة (−2.94 ± 1.55 مقابل −0.95 ± 1.83٪، p = 0.016).
في هذه الورقة، خلص رحمييل وآخرون إلى أن "علاج AAT كان آمنًا وجيد التحمل لدى الأطفال المصابين بمرض السكري المناعي الذاتي الذي تم تشخيصه حديثًا. تجدر الإشارة إلى أن هذه هي الدراسة الأولى التي تثبت سلامة عالية في استخدام جرعات مختلفة من AAT تعطى عن طريق التسريب للأطفال الذين لا يعانون من مرض نقص الجينات ألفا -1 (AATD) والذين يعانون من النوع الأول الذي تم تشخيصه حديثا مرض السكري، مع الحفاظ على توازن نسبة السكر في الدم وانخفاض أقل في مستويات الببتيد C.
"نحن سعداء بهذه البيانات الإيجابية المنشورة في مجلة Pediatric Diabetes لأنها تؤكد صحة نتائج الدراسات السابقة التي تظهر أن علاج AAT يمكن أن يقلل من العلامات المسببة للالتهابات وقد يحمي خلايا البنكرياس من تفاعلات المناعة الذاتية لدى مرضى السكري الذين تم تشخيصهم حديثًا كما تم قياسها بمستويات HbA1C و C - الببتيد"، أشار أمير لندن، الرئيس التنفيذي لشركة كامادا. "نحن نواصل تجنيد المرضى في المرحلة 2/3 من تجربة AAT لدى مرضى السكري من النوع الأول الذين تم تشخيصهم حديثًا، ونتطلع إلى إحراز تقدم في هذه التجربة المهمة، والتي نعتقد أنها قد تغير طريقة علاج مرض السكري من النوع الأول."

תגובה אחת
أعجبني نظام محاكاة العظام نظام ممتاز وفيه مجال للتحسين والاستفادة. ممتاز