مقابلة مع البروفيسور مشنا غاليا مين، رئيس مختبر الكيمياء الحيوية في التخنيون / بقلم: يائيل هافمان كوهين

في السنوات الأخيرة، تم افتتاح مختبر للكيمياء الحيوية في كلية الكيمياء في التخنيون، تحت قيادة البروفيسور المشارك جاليا ماعين. في مشهد ابتكار المحاكاة الحيوية، والذي أصبح اليوم أكثر ارتباطًا بالتطورات الهندسية على مستويات عالية من التقليد مثل تقليد الأعضاء أو الكائنات الحية وأقل ارتباطًا بالتطورات الكيميائية، يبرز هذا المختبر، الذي يتعامل مع تقليد المحاكاة الحيوية على المستوى الجزيئي. وتبين أنه حتى على المستوى الجزيئي هناك بحث وتقليد للوظائف والإجراءات المتعلقة بالهياكل، والنتيجة هي الابتكار.
يتعامل المختبر مع العديد من التطورات المحاكاة الحيوية بناءً على الكيمياء الأساسية.
يتناول المشروع الأول التحفيز الأنزيمي الحيوي. يعتمد المشروع على دراسة المجلدات، وهي الجزيئات التي يمكن طيها في المحلول عن طريق تكوين روابط غير تساهمية. يمكن أن تحتوي المجلدات على بنية حلزونية، على سبيل المثال، والتي تحاكي البنية الحلزونية الموجودة في البوليمرات الطبيعية، مثل الببتيدات والبروتينات. يتيح هذا الهيكل المطوي نشاط البروتينات، مثل، على سبيل المثال، التحفيز الانتقائي للتفاعلات.
في المختبر، تم تطوير جزيء يشبه الببتيد، والذي ينظم نفسه على شكل حلزون (يمين أو يسار). لقد ربطوا به محفزًا يعرف كيفية أكسدة الكحول. المحفز بلا اتجاه. عند توصيله بالملف، يتلقى المحفز اتجاهًا من الملف، ويكون قادرًا على تحفيز الجزيء الأيمن (أو الأيسر) بشكل انتقائي وترك الجزيء الأيسر (أو الأيمن) في المحلول. وهكذا يتم الفصل بين الكحل الأيمن والأيسر الذي في الخليط.
التطبيقات الممكنة: في عمليات تخليق الجزيئات، حيث يكون الفصل بين أزواج الجزيئات مطلوبًا ويلزم وجود محفز لفصلها في تطبيقات مختلفة. في عمليات إنتاج الدواء، على سبيل المثال، تكون هناك حاجة إلى جزيئات ذات اتجاه محدد (على سبيل المثال، الجزيء ذو الاتجاه الصحيح فقط هو الدواء، في حين أن الجزيء ذو الاتجاه الأيسر يكون غير نشط، أو حتى ضارًا)، في حين أن عملية التخليق في كثير من الأحيان تنتج مخاليط، لذلك يلزم الفصل.
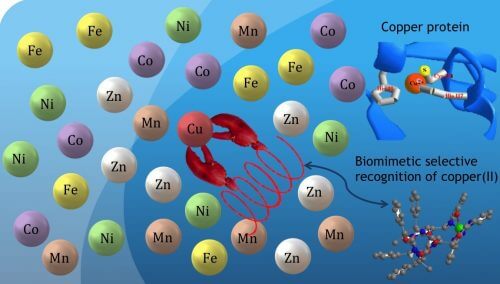
ويتناول المشروع الثاني الانتقائية المحاكاة الحيوية. ترتبط الجزيئات المختلفة في أجسامنا أو في الطبيعة فقط بأيونات معدنية محددة (على سبيل المثال أيونات النحاس) من مجموعة متنوعة من الأيونات المعدنية (الحديد والزنك والمغنيسيوم وما إلى ذلك) لعملها. في المختبر، قاموا بإنشاء جزيء يشبه الحلزون، يحتوي على وحدتين متصلتين بنفس الجانب من الحلزون، والذي يمكنه التقاط أيونات النحاس فقط من "بحر" الأيونات المعدنية (انظر الصورة 1 الذي يحاكي العملية). قد تكون التطبيقات المستقبلية لهذا في عالم الطب. على سبيل المثال، ترتبط الأمراض المرتبطة بعدم كفاية نشاط الدماغ في الشيخوخة، مثل الخرف، بتراكم زائد للأيونات المعدنية مثل النحاس والزنك والحديد والألمنيوم. التطوير المستقبلي لانتقائية المحاكاة الحيوية قد يسمح بالتقاط انتقائي لهذه الأيونات وإزالتها من الجسم.
أما المشروع الثالث فيتناول تسريع التفاعلات المحاكاة الحيوية. يعرف نظام التمثيل الضوئي الذي يعمل في النباتات والطحالب كيفية إنتاج الطاقة من ضوء الشمس، وإذا نجحنا في تقليدها، يمكننا التعامل مع مشكلة الطاقة المستنفدة باستمرار. ويتكون النظام من جزأين: جزء يمتص ضوء الشمس والماء، ويؤكسد الماء بالطاقة الشمسية، وينتج الأكسجين والبروتونات والإلكترونات. الجزء الثاني يأخذ البروتونات والإلكترونات وينتج منها الهيدروجين والسكر (مصادر الطاقة).
وفي المختبر تم تصنيع جزيء يشبه في بنيته مركبا يحتوي على أيونات المنغنيز، التي تعتبر محفزا في عملية أكسدة الماء. تم تصميم الجزيء ليكون قابلاً للذوبان في الماء، بحيث يكون من الممكن التحقق مما إذا كان يمكنه تحفيز أكسدته من خلال إمكانات كهربائية منخفضة (ميزة بيئية). وفي الواقع، وجد أن الجزيء قابل للذوبان ومستقر في الماء، مما يظهر القدرة على إنتاج إلكترونات أكثر مما تم استثماره فيه إلى جانب مستويات عالية من الأكسجين. التطبيقات الممكنة: إنتاج الهيدروجين كبديل "أخضر" ومتوفر للغاز كمصدر للطاقة.
أما المشروع الرابع فيتناول المحفزات العاملة في التعاونيات. يمكن للإنزيم تسريع العملية 600,000 مرة أسرع، وهذا عند درجة حرارة الجسم والضغط الجوي للبيئة المعيشية. للمقارنة، اليوم في الصناعة (على سبيل المثال: أكسدة الكحوليات، أكسدة الميثانول إلى الميثانول، إنتاج الأمونيا) تستخدم المحفزات التي تعمل عند درجة حرارة 500 درجة وتحت ضغوط عالية جدا.
وتبين أن أحد المبادئ البارزة في عملية التسارع الطبيعي هو مبدأ التعاون. يحتوي كل إنزيم على موقع نشط واحد على الأقل، وهو الموقع الذي تحدث فيه عملية تحفيز تفاعل معين. يحتوي هذا الموقع على 2-3 أحماض أمينية، وغالبًا أيضًا أيون أو أيونات معدنية. على الرغم من أن واحدًا فقط من الأحماض الأمينية أو أيون المعدن يتصل فعليًا بالجزيء الذي تحول إلى جزيء محفز آخر، فإن الباقي يساعد في العملية - على سبيل المثال، يعمل على تثبيت الحمض الأميني أو حالة أكسدة أيون المعدن.
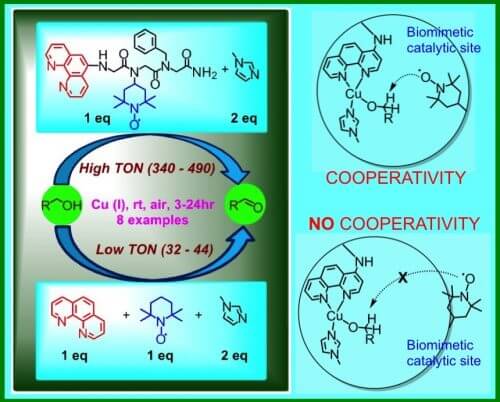
في المختبر، قاموا بتقليد ميزة المشاركة، وأظهروا أنه إذا أخذت محفزين مختلفين يعملان في المحلول بطريقة تعاونية، وقمت بتثبيتهما على جزيء آخر بحيث يتم إنشاء "موقع نشط"، فإن التعاون يزداد بشكل كبير ويزداد التفاعل. يمكن زيادة كفاءة التفاعل المحفز 20-25 مرة (انظر الصورة 2 تظهر هذه العملية).
ويبدو أن هناك الكثير من إمكانات الابتكار على المستوى الجزيئي، وأننا سنسمع المزيد في السنوات القادمة عن الكيمياء الحيوية.
تمت كتابة الخبر بعد مقابلة مع البروفيسور المساعد جاليا مين، رئيس مختبر الكيمياء الحيوية في التخنيون.
