زيادة تغلغل المواد السامة في الدماغ يمكن أن يسبب مرض الزهايمر. قد يؤدي هذا الاكتشاف الجديد إلى تطوير أدوية جديدة تمامًا لهذا المرض الخطير.
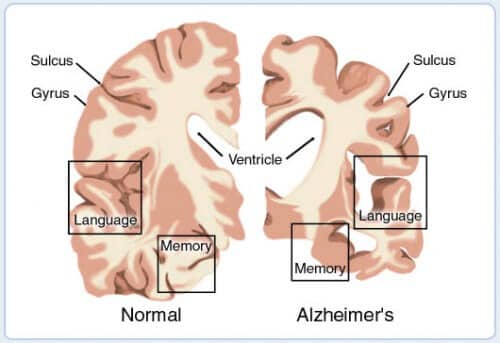
يصيب مرض الزهايمر عادة الأشخاص الذين تزيد أعمارهم عن 65 عامًا. وهو مرض خطير يصاحبه انحطاط خلايا الدماغ وفقدان الذاكرة. كما يشكل المرض عبئا ثقيلا على الأسرة الحاضنة، فهو غير قابل للشفاء ويسبب الوفاة. مر البحث حول تطور المرض بعدة منعطفات. في البداية كان يُعتقد أن الخلايا المتدهورة هي في الأساس خلايا تنتج الناقل العصبي الأسيتيل كولين، وأن نقص الأسيتيل كولين يسبب المرض. يتم تكسير الأسيتيل كولين في الجسم والدماغ بواسطة إنزيم يسمى أستيل كولينستراز (AChE)، لذا فإن العلاجات الأولى التي تم تطويرها تمنع نشاط الإنزيم وتزيد من تركيز الأسيتيل كولين في الدماغ. إلا أن تأثير العلاجات يكون جزئيا ومحدودا زمنيا، ولا يؤخر تدهور المرض. نحن نعلم اليوم أن الخلايا العصبية التي تنتج الغلوتامات، وهو الناقل العصبي الرئيسي في الدماغ الذي يسبب تنشيط الخلايا العصبية الأخرى، تتدهور أيضًا، كما يحدث أيضًا انحطاط للخلايا العصبية الأخرى. ولهذا السبب، فإن العلاجات الدوائية الأحدث لمرض الزهايمر تنظم أيضًا نشاط الغلوتامات، وليس الأسيتيل كولين فقط، ولكنها أيضًا لا تؤثر على مسار المرض.
إذا كان الأمر كذلك، ما هو سبب مرض الزهايمر؟ في أدمغة مرضى الزهايمر، تظهر رواسب (تسمى لويحات) من جزء البروتين المعروف باسم أميلويد بيتا، ويُعتقد على نطاق واسع أن هذه اللويحات هي أسباب تنكس الخلايا العصبية. ولكن في الواقع سبب المرض غير معروف حقا. ومع ذلك، فإن علم الوراثة يوفر دليلًا واحدًا مهمًا، على شكل جين يشفر بروتينًا يسمى البروتين الدهني E (APOE). يزيد أحد المتغيرات (أو الأليلات) لهذا الجين، APOE4، ما يصل إلى 12 مرة من خطر الإصابة بمرض الزهايمر في سن الشيخوخة (على عكس مرض الزهايمر العائلي، وهو مرض نادر جدًا يمكن أن يظهر نفسه بالفعل في الثلاثينيات من العمر). مرضى).
إذن ما هو بروتين APOE؟ وهو بروتين ينتمي إلى مجموعة البروتينات التي ترتبط، من بين أشياء أخرى، بالمواد الدهنية، مثل الكوليسترول. كشفت الأبحاث الحديثة أن جميع متغيرات البروتين، وخاصة APOE4، لها دور حاسم في حماية الدماغ. قد تغير النتائج الطريقة التي نفهم بها مرض الزهايمر، بل وتساهم في تطوير أدوية جديدة تمامًا لهذا المرض.
تختلف الأوعية الدموية التي تزود الدماغ بالدم عن بقية الأوعية الدموية في الجسم. وهي تقريبًا منيعة تجاه المواد التي تتدفق في الدم، ولكنها تنقل فقط جزيئات صغيرة من المواد التي يحتاجها الدماغ. يُطلق على البنية الخاصة للأوعية الدموية في الدماغ اسم الحاجز الدموي الدماغي، والغرض منه هو حماية الخلايا العصبية في الدماغ من المواد الضارة التي قد تصل عبر مجرى الدم. الحاجز الدموي الدماغي هو السبب وراء عدم وصول العديد من الأدوية إلى الدماغ.
في مايو 2012، نُشرت مقالة في مجلة Nature، تناقش أدوار وتأثيرات APOE4 على حاجز الدم في الدماغ. تم إجراء البحث على الفئران (نعم، مرة أخرى تجارب على الحيوانات لصالح البشرية)، حيث تم إزالة الجين الفأري لـ APOE باستخدام طرق الهندسة الوراثية، وتم إدخال الجين البشري لـ APOE4 مكانه. واتضح للباحثين أن الحاجز الدموي الدماغي في هذه الفئران قد تضرر وأن المواد السامة اخترقت الدماغ. قام الباحثون بالتحقيق في الآليات الجزيئية وتمكنوا من استخدام الأدوية لإصلاح الأضرار التي لحقت بالحاجز الدموي الدماغي، بحيث لم تعد المواد السامة تدخل الدماغ.
لكن النتيجة الأكثر أهمية أظهرت أنه عندما يتضرر الحاجز الدموي الدماغي وتخترق المواد السامة، يحدث تلف في الخلايا العصبية في الدماغ يشبه مرض الزهايمر. ومن المثير للاهتمام أنه عندما أعطينا المواد التي أصلحت الحاجز الدموي الدماغي، توقفت الخلايا العصبية عن الموت وكان هناك تعافي. هل من الممكن أن السبب الرئيسي لمرض الزهايمر ليس أميلويد بيتا، بل تلف الحاجز الدموي الدماغي؟ وإذا كان الأمر كذلك، فهل سيكون من الممكن علاج مرض الزهايمر (على الأقل في المراحل المبكرة من المرض) عن طريق علاج الحاجز الدموي الدماغي؟ ولا شك أن هذا البحث يفتح طريقة جديدة للتفكير. هناك حوالي 100,000 مريض بالزهايمر في إسرائيل وعدة ملايين في العالم. انضمت مجموعات بحثية مختلفة بالفعل إلى الاتجاه البحثي الجديد. هل يمكن أن نتمكن أخيرًا من مساعدة هؤلاء المرضى؟
والمزيد حول هذا الموضوع
يتحكم صميم البروتين الشحمي E في سلامة الأوعية الدموية الدماغية عن طريق السيكلوفيلين A، روبرت د. بيل وزملاؤه في الطبيعة, المجلد 485، الصفحات 512-516 (24 مايو 2012)
عن المؤلف
يتسحاق فيرنز هو أستاذ في قسم علم الأعصاب في الجامعة العبرية في القدس، ومؤسس الجمعية الإسرائيلية لعلم الأعصاب ومؤسس مختبرات بلمونت للشباب في القدس.

תגובה אחת
حتى ينشروا الدراسات ويجبروا المجتمع الغربي على العمل على تغيير متوسط العمر المتوقع،
لن يكون هناك حلول للأمراض التي تبدأ من سوء التغذية وضعف النشاط البدني (الكسل) والحياة المادية،
سيستمر المرض...
يحتاج الطب الغربي أن يتعلم أنه لا يوجد شيء اسمه اختراع حبة معجزة تغير الإنسان دون أن يغير نفسه.