تغير النتائج الجديدة طريقة تفكيرنا في استقلاب الحديد. أجريت الدراسة من قبل باحثات في التخنيون بالتعاون مع زملاء من أربعة دول في الخارج
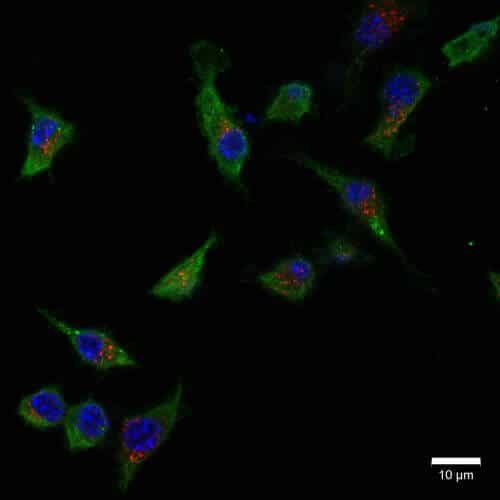
تعرض مجلة "دم" في غلاف عددها الأخير، الذي صدر في 18 كانون الثاني/يناير، دراسة أجرتها الدكتورة ماريانا ترومان-روزنزفيت والأستاذة المشاركة إستر ميرون-هولتز من كلية التكنولوجيا الحيوية والهندسة الغذائية في التخنيون. وتقدم الدراسة لأول مرة آلية نقل وإفراز الفيريتين، وهو البروتين الذي كان حتى الآن يعتبر أساسيا لتخزين الحديد في جسم الإنسان. تغير هذه الدراسة الرئيسية طريقة تفكيرنا حول نقل الحديد في الجسم وتفتح قنوات جديدة للبحث وتطوير علاجات مستقبلية للعديد من الأمراض.
الحديد هو عنصر أساسي لحسن سير العمل في معظم الكائنات الحية. وهو مسؤول عن نقل الأكسجين في خلايا الدم الحمراء، وتنشيط الإنزيمات المرتبطة بتكوين الحمض النووي وإنتاج الطاقة في الميتوكوندريا في الخلية. نقص الحديد يضر بنقل الأكسجين إلى جميع أجزاء الجسم وانقسام الخلايا وإنتاج الطاقة في الخلية. الحديد الزائد والحديد "العاري"، أي الحديد غير المغلف بأي بروتين، قد يؤدي إلى الإجهاد التأكسدي الذي يمكن أن يضر بالكائن الحي. وبالتالي فإن النقص أو الزيادة في توازن الحديد قد يؤدي إلى تطور الأمراض الالتهابية والسرطان والأمراض العصبية مثل مرض الزهايمر ومرض باركنسون.
ويعتبر بروتين الفيريتين أحد العوامل الأساسية في تنظيم مستوى الحديد الخلوي وحماية الجسم من التسمم بالحديد. توضح المقالة توزيع الفيريتين داخل الخلية وآليات إفرازه خارج الخلية. وبحسب البروفيسور ميشنا ميرون هولتز، فإن "الفيريتين هو بروتين مهم لتوازن الحديد في الجسم، وهناك علاقة قوية بين الاضطرابات في توازن الحديد والفيريتين ومختلف الظواهر المرضية والعصبية". تتيح النتائج التي توصلنا إليها فهمًا أكثر دقة ومتعمقًا لخصائص الفيريتين والعمليات الجزيئية الأساسية التي يخضع لها. إن مثل هذا الفهم له أهمية كبيرة لأنه قد يساهم في تطوير علاجات للعديد من الأمراض العصبية التنكسية، والتي تتميز بتوزيع غير طبيعي للحديد في الدماغ.
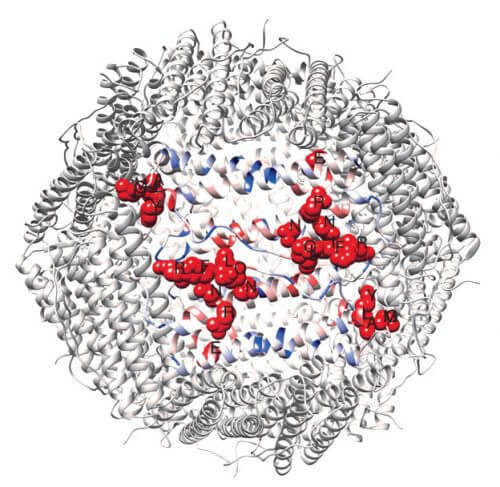
ركزت الدراسة المنشورة في مجلة Blood على توصيف التوزيع داخل الخلايا وإفراز الفيريتين من الخلايا البلعمية، وهي خلايا من الجهاز المناعي تلعب دورًا مركزيًا في الدورة الدموية الجهازية للحديد. وتضمنت الدراسة استخدام أدوات المعلومات الحيوية لدراسة تطور إفراز الفيريتين، وبنيته المكانية، بالإضافة إلى الطبولوجيا التي قد تكون مرتبطة بتوزيع الفيريتين. "لقد سمح لنا استخدام هذه الأدوات بالتنبؤ بالمناطق الموجودة على سطح الفيريتين والتي تلعب دورًا في إفرازه. وبمساعدة طرق كيميائية حيوية متنوعة، بالإضافة إلى تقنية CRISPR-Cas9 التي تتيح التحرير السريع للجينوم، اكتشفنا أن الضرر الذي يلحق بمواقع معينة على سطح الفيريتين يغير إفرازه"، تقول الأستاذة المشاركة إستر ميرون هولتز.
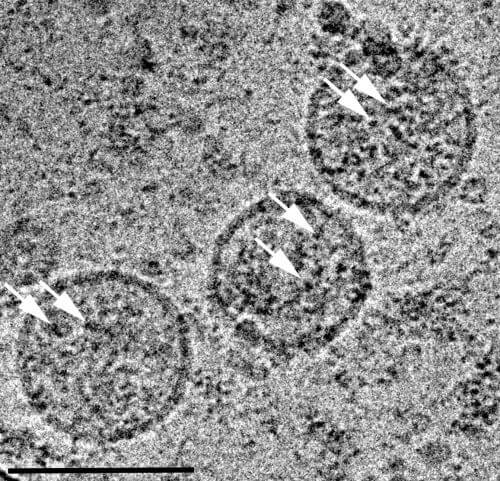
ويكشف المقال أن الفيريتين يتم إفرازه بواسطة آليتين غير تقليديتين للإفراز، حيث يتم إحداهما من خلال حويصلة نانومترية تسمى الإكسوسوم. وفقًا للدكتور ترومان روزنزفيت، "تدرس العديد من المجموعات البحثية حاليًا ديناميكيات نقل المواد في الإكسوسومات - وهي منصة تسمح لهذه المواد باختراق حاجز الدم في الدماغ. يُظهر المنشور الحالي، لأول مرة، أن الفيريتين الذي يحتوي على آلاف ذرات الحديد موجود في الإكسوسومات خارج الخلية. لا يزال من غير الواضح ما هي وظيفة هذا الفيريتين، لكننا نقدر أن الفيريتين له دور رئيسي في توزيع الحديد بين الخلايا في الأنسجة مثل الدماغ، وليس فقط في التخزين الآمن والمتاح للحديد داخل الخلية. " إن اكتشافات الدراسة الحالية تضع الفيريتين في طليعة عملية التمثيل الغذائي النظامي للحديد، وتكشف أن الفيريتين لا يخزن الحديد فحسب، بل ينقله أيضًا بطريقة خاضعة للرقابة، وفي الواقع يعمل كجهاز تحكم مركزي للحديد في الجسم.
عن الباحثين
بروفيسور مشارك إستر ميرون هولتز، ولدت في سويسرا، درست علوم التغذية في كلية الزراعة وحصلت على درجة الماجستير والماجستير في قسم التغذية البشرية في كلية الطب في الجامعة العبرية تحت إشراف البروفيسور أ.م. كونين والبروفيسور ي. الراحل ميتسنر. قامت بأبحاث ما بعد الدكتوراه في المعاهد الوطنية للصحة (NIH)، وفي عام 2005 هاجرت إلى إسرائيل مرة أخرى ومنذ ذلك الحين ترأس مختبر التغذية الجزيئية في التخنيون. يتم في المختبر دراسة التحكم في توازن الحديد في الأعضاء المختلفة ودوره في تطور العمليات المرضية المؤدية إلى أمراض الأمعاء الالتهابية ومشاكل الخصوبة عند الذكور وغيرها. بعد المقال في الدم، سيواصل الباحثون المختبريون دراسة دور الفيريتين المفرز في الكائن الحي السليم وفي الأمراض المختلفة وتطوير أساليب التدخل العلاجي في توزيع الحديد في الأنسجة.
تخرج الدكتور ترومان روزنزفيت بدرجة البكالوريوس في علم الأحياء من التخنيون والتحق بالبحرية كضابط أبحاث. أثناء خدمتها العسكرية في معهد الطب البحري، قامت بدراسة سمية الأكسجين في الدماغ باستخدام خلايا الضغط البحثية. في الوقت نفسه، حصلت على درجة البكالوريوس الإضافية في التكنولوجيا الحيوية والهندسة الغذائية في التخنيون ثم حصلت على الدكتوراه المباشرة تحت إشراف الأستاذ المشارك ميرون هولتز. تم مؤخرًا قبول الدكتورة ماريانا ترومان روزنزفيت في البرنامج الوطني لعلم السموم في الولايات المتحدة الأمريكية، وهي تعمل حاليًا على إيجاد التمويل لدراسات ما بعد الدكتوراه. ووفقا لها، "خلال فترة الدكتوراه، تطوعت بالفعل في المعاهد الوطنية للصحة في الولايات المتحدة الأمريكية بفضل إستر، وقد أوضحت لي إقامتي هناك مدى أهمية التعرض للأبحاث التي أجريت في الخارج. المعهد الذي سأدرس فيه بعد الدكتوراه يعتبر رائدا في مجال علم السموم في العالم وأعتزم الدراسة والبحث والتطوير هناك قدر الإمكان وجلب كل المعرفة إلى إسرائيل."

תגובה אחת
لمن هذه المقالة؟
فقط لأطباء الدم؟
كم منهم يزور موقع العلوم؟
لماذا لا تحاول التبسيط قليلاً حتى يفهم المزيد من القراء ما يدور حوله؟