ولا يقتصر الأمر على البكتيريا اليائسة فحسب، بل حتى الخلايا السرطانية التي تواجه الانقراض قد تنشط استجابة SOS وتطور مقاومة للأدوية
قد يختار الإنسان اليائس طرقًا يائسة، وهذا لا ينطبق على البشر فقط. قبل خمسة عقود، تم اكتشاف أن البكتيريا التي تتعرض لتهديد وجودي تقوم بتنشيط برنامج طوارئ وراثي، خطير ولكنه فعال، يسمى "استجابة SOS". لقد اكتشفوا ذلك مؤخرًا علماء معهد وايزمان للعلوم أنه حتى الخلايا السرطانية اليائسة تنشط استجابة SOS التي تساعدها على تطوير مقاومة للأدوية المضادة للسرطان. وطور الباحثون طريقة لعرقلة آلية SOS لدى الفئران، مما قد يؤدي إلى تطوير علاج جديد لدى البشر.
الفريق البحثي بقيادة البروفيسور . يوسف الأردن من قسم المناعة والتجديد البيولوجي بالمعهد، قام بدراسة نوع فرعي من سرطان الرئة، وهو سمة من سمات المرضى الذين لا يدخنون. هناك لغز يحيط بهذا السرطان، ليس فقط لأنه لا علاقة له بالتدخين، ولكن أيضا لأن معدل الإصابة به يختلف كثيرا في أجزاء مختلفة من العالم. على سبيل المثال، في إسرائيل والولايات المتحدة يمثل حوالي 12% من جميع حالات سرطان الرئة، بينما في دول شرق آسيا يبلغ معدل انتشاره بين مرضى سرطان الرئة أكثر من 35%.
ويوجد حاليًا العديد من الأدوية الفعالة لعلاج أورام الرئة هذه، والتي تتميز بحدوث طفرات في الجين المسمى EGFR. ومع ذلك، بعد حوالي عام، تكتسب الأورام مقاومة، وتتوقف الأدوية عن العمل. في هذه المرحلة، سيتلقى المرضى أدوية الجيل الثاني والثالث، ولكن في النهاية سيطور الورم مقاومة لكل منهما.
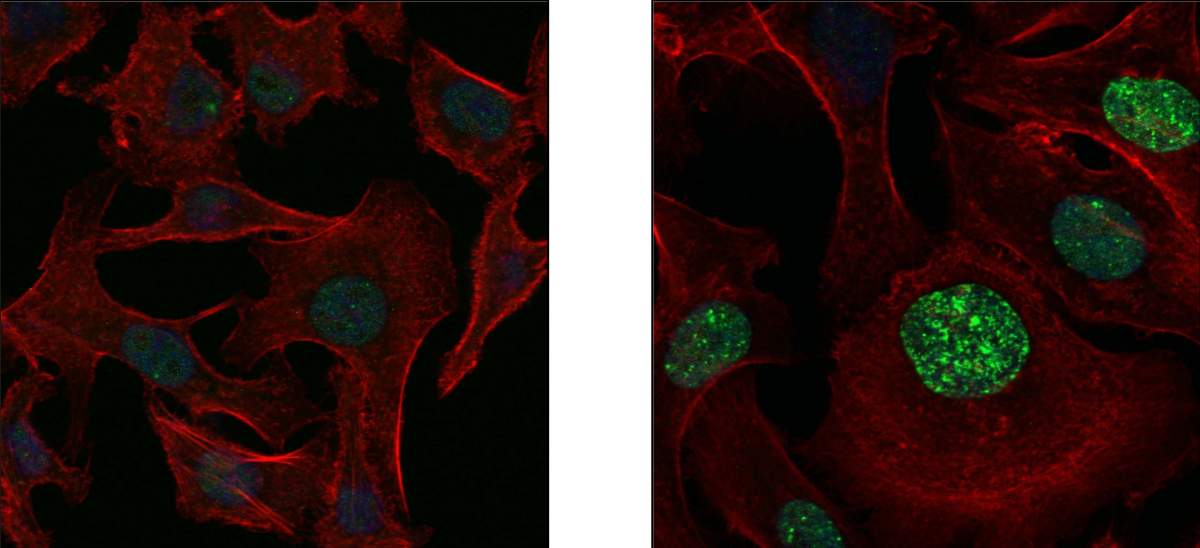
"أردنا أن نفهم كيفية تطور المقاومة لنتعلم كيفية الوقاية منها"، يوضح البروفيسور جوردان، الذي استلهم البحث من مصدر مفاجئ - البكتيريا. في عام 1975، اكتشف عالم الأحياء الكرواتي ميروسلاف ريدمان أن التعرض للمواد الكيميائية السامة أو المضادات الحيوية أو الأشعة فوق البنفسجية يؤدي إلى قيام البكتيريا بإحداث العديد من الطفرات على طول الحمض النووي الخاص بها. "عندما تم اكتشاف استجابة SOS لأول مرة، واجه العلماء صعوبة في تصديق أنها حقيقية. هل تنتج البكتيريا عن قصد الكثير من الطفرات؟ يقول البروفيسور جوردان: "بعد كل شيء، فإن الطفرات نفسها تعرضهم للخطر". "لكن استجابة SOS يتم تنشيطها فقط عندما تواجه البكتيريا خطر الانقراض، ومن ثم يدفعها ثمن المخاطرة بحيث يكون لدى بعضها على الأقل مقاومة للتهديد الوجودي."
أثبت اتجاه هذا البحث نفسه: اكتشف البروفيسور جوردان وزملاؤه أنه تحت هجوم الأدوية المضادة للسرطان، تتطور المقاومة في أورام الرئة هذه من خلال آلية مشابهة لاستجابة SOS في البكتيريا. تم الحصول على النتائج بمساعدة التجارب التي أجريت على أنسجة الورم المزروعة وعلى الفئران، بقيادة الدكتور أشيش نورونها، الذي كان آنذاك طالبًا بحثيًا في مختبر البروفيسور جوردان، وبالتعاون مع فريق كبير من العلماء والأطباء من إسرائيل وأوروبا. والولايات المتحدة.
اكتشف الباحثون كيف تعمل نسخة SOS من السرطان بكل تفاصيلها الجزيئية. عندما يتم تدمير العديد من الخلايا السرطانية، فإن البقايا التي تتركها وراءها تنشط في الخلايا السرطانية المتبقية آلية تؤدي إلى استبدال الإنزيمات المسؤولة عن نسخ الحمض النووي في نواة الخلية. فبدلاً من الإنزيمات الدقيقة التي تقوم بعملية النسخ بدقة كبيرة، بما في ذلك تصحيح الأخطاء، يتم تنشيط الإنزيمات المهملة عمداً، مما يؤدي إلى إنتاج العديد من الطفرات في كل مرة تنقسم فيها الخلية. بالإضافة إلى الإنزيمات المهملة، يتم أيضًا تنشيط آلية تعطل الإمداد المناسب لوحدات البناء الضرورية لنسخ الحمض النووي: النيوكليوتيدات A وT وG وC. تنتج هذه الآلية فائضًا في زوج واحد من النيوكليوتيدات، G + A، مقارنة بالزوجين الآخرين، مما يؤدي إلى حدوث أخطاء إضافية في عملية النسخ.
""عندما تم اكتشاف استجابة SOS لأول مرة، واجه العلماء صعوبة في تصديق أنها حقيقية. هل تنتج البكتيريا عن قصد الكثير من الطفرات؟ ففي نهاية المطاف، فإن الطفرات نفسها تعرضهم للخطر.
والأهم من ذلك، أن العلماء تمكنوا من تحديد المنشط الرئيسي لاستجابة SOS في الورم: المستقبل الخلوي المسمى AXL. يعمل هذا المستقبل المعبر عنه على سطح غشاء الخلية كجهاز استشعار يستقبل الإشارات من الخلايا السرطانية الميتة وكمفتاح رئيسي لتنشيط الآليات اللازمة لإنشاء الطفرات. مفعوله سريع وتأثيره سيء: خلال عام من بدء العلاج الدوائي، قد تحتوي جميع الخلايا الموجودة في الورم على طفرات تمنحها المقاومة.
بعد هذه النتائج، شرع العلماء في إيجاد طرق لمنع استجابة السرطان للطوارئ. ووجدوا أنه عندما يزيلون مستقبل AXL في الخلايا السرطانية، يمكنهم منع ظهور مقاومة الأدوية. "لقد كانت" يوريكا! " "لقد أدركنا أننا بحاجة إلى البحث عن علاج يحيد هذا المستقبل"، يقول البروفيسور جوردان.
لكن المهمة كانت أصعب مما توقعت. ونجح الباحثون في إنشاء جسم مضاد يحجب AXL في الفئران، لكنه لم يكن فعالا بما فيه الكفاية، لا عندما يُعطى بمفرده ولا بالاشتراك مع عقار Tagriso المستخدم لعلاج سرطان الرئة الذي يتميز بطفرات في جين EGFR. فقط عندما استخدم الباحثون علاجًا ثلاثيًا - الجسم المضاد تاجريسو ودواء آخر مضاد للسرطان - أربيتوكس، تم تطويره على أساس بحث البروفيسور جوردان والبروفيسور الراحل مايكل سيلا - عندها فقط ظهرت إمكانية تطوير مقاومة الأدوية تم حظرها واختفت الأورام إلى الأبد.
قد تمهد نتائج البحث الطريق لعلاج واعد لسرطان الرئة لدى المرضى غير المدخنين، وربما أيضًا في أنواع أخرى من السرطان حيث تتطور مقاومة الأدوية الموجودة. ومع ذلك، سيستغرق الأمر عدة سنوات لتطوير الأجسام المضادة لمستقبل AXL في البشر وإجراء تجارب سريرية للعلاج الثلاثي.
وشارك في الدراسة أيضًا الدكتور نيشانث ناثراج، والدكتور موشيت ليندزن، والدكتور سوما غوش، والدكتور أرتورو سيموني نيفيس، وآكنيشكا فيرما، وريشيتا تشاترجي، وأرونشالام سيكار، والدكتور سواندو جيري، وديانا، ودراغو جارسيا من قسم علم المناعة. والتجديد البيولوجي لمعهد وايزمان للعلوم؛ والدكتور ويلز روبنسون، والدكتور سانجو سينها، والبروفيسور إيثان روبين من المعهد الوطني للسرطان بالولايات المتحدة الأمريكية؛ الدكتور بيني جيتوميرسكي، والدكتور يارا أورين، والدكتور بريان دانيش، وجديوفور أزيك، والبروفيسور جاد جيتز من المعهد العريض لمعهد ماساتشوستس للتكنولوجيا وجامعة هارفارد؛ سارة أوستر والبروفيسور رامي عقيلان من الجامعة العبرية في القدس؛ الدكتور سابتابارنا موخيرجي والبروفيسور موشيه أورين من قسم بيولوجيا الخلايا الجزيئية بالمعهد؛ الدكتور راينر فايل، والدكتور سيمون بورجوني، والبروفيسور ستيفان وايمان من المركز الألماني لأبحاث السرطان (DKFZ)؛ والدكتور ألكسندر برانديس من قسم البنى التحتية لأبحاث علوم الحياة بالمعهد؛ ولوكاس كير، والدكتور وي وو، والدكتور كولين بلاكلي، والدكتور تريفور بيفن من جامعة كاليفورنيا، سان فرانسيسكو؛ والدكتور يونغمين تشونغ والدكتور جو سانغ لي من جامعة سينغكيونكوان في كوريا؛ البروفيسور ماتيا لوريولا، والبروفيسور مايكل أنجلو فيورنتينو، والبروفيسور أندريا أرديزوني من جامعة بولونيا في إيطاليا؛ والدكتور لاشمي فريدة من معهد أبحاث IBM في ولاية نيويورك بالولايات المتحدة الأمريكية؛ البروفيسور جوان بروغي من كلية الطب بجامعة هارفارد؛ والبروفيسور أفيف ريجيف من شركة جينينتيك بالولايات المتحدة الأمريكية.
