ألقى باحثون من جامعة تل أبيب الضوء على لغز عمره 140 عامًا في مقال نشر في مجلة Nature. يظهر البحث لأول مرة كيف يمكن لعدد غير طبيعي من الكروموسومات (اختلال الصيغة الصبغية) - وهي سمة فريدة من نوعها للخلايا السرطانية المعروفة للباحثين منذ عقود - أن تصبح نقطة ضعف في هذه الخلايا. قد يؤدي البحث في المستقبل إلى تطوير أدوية تستفيد من نقطة الضعف هذه لاستهداف الخلايا السرطانية
ما الذي يجعل الخلايا السرطانية مختلفة عن الخلايا الطبيعية في الجسم؟ وهل يمكن استخدام هذا التفرد للإضرار بهم وشل عملهم؟ لقد أزعج هذا السؤال الأساسي الباحثين في مجال السرطان منذ منتصف القرن التاسع عشر وحتى يومنا هذا، ويعد البحث عن الخصائص الفريدة للخلايا السرطانية لبنة أساسية في أبحاث السرطان الحديثة. أظهرت دراسة جديدة أجراها باحثون من جامعة تل أبيب لأول مرة كيف يمكن أن يصبح عدد غير طبيعي من الكروموسومات (اختلال الصيغة الصبغية) - وهي سمة فريدة من نوعها للخلايا السرطانية المعروفة للباحثين منذ عقود - نقطة ضعف في هذه الخلايا. قد يؤدي البحث في المستقبل إلى تطوير أدوية تستفيد من نقطة الضعف هذه لاستهداف الخلايا السرطانية.
تم إجراء البحث، الذي نُشر في مجلة Nature المرموقة، في مختبر الدكتور أوري بن دافيد من كلية الطب ساكلر في جامعة تل أبيب، بالتعاون مع 6 مختبرات من 4 دول أخرى (الولايات المتحدة الأمريكية، ألمانيا، هولندا وإيطاليا).
اختلال الصيغة الصبغية هو السمة المميزة للسرطان. في حين أن الخلايا البشرية الطبيعية تحتوي على مجموعتين من 23 كروموسوم، واحدة من الأب وواحدة من الأم، فإن الخلايا المختلة الصيغة الصبغية لها عدد مختلف من الكروموسومات. عندما يحدث اختلال الصيغة الصبغية في الخلايا السرطانية، لا تستطيع الخلايا "تحمله" فحسب، بل يمكنها أيضًا تعزيز عملية السرطان. لقد تم اكتشاف العلاقة بين اختلال الصيغة الصبغية والسرطان قبل ما يقرب من 140 عاما، أي قبل وقت طويل من فهم أن السرطان مرض وراثي (وحتى قبل اكتشاف الحمض النووي باعتباره مادة وراثية).
وفق دكتور بن دافيد، اختلال الصيغة الصبغية هو في الواقع التغير الجيني الأكثر شيوعًا في السرطان. حوالي 90% من الأورام الصلبة، مثل سرطان الثدي وسرطان القولون، و75% من سرطانات الدم، تكون مختلة الصيغة الصبغية. ومع ذلك، فإننا لا نفهم إلا إلى حد محدود كيف تساهم هذه الظاهرة في تطور وانتشار السرطان.
كجزء من الدراسة، طبق الباحثون أساليب المعلوماتية الحيوية (الحسابية) المتقدمة من أجل تحديد موقع اختلال الصيغة الصبغية بين حوالي ألف من مزارع الخلايا السرطانية. ثم قارن الباحثون الحساسيات الوراثية للخلايا ذات المستوى العالي من اختلال الصيغة الصبغية مع تلك الموجودة في الخلايا ذات المستوى المنخفض، بالإضافة إلى حساسيتها لمختلف الأدوية والمواد الكيميائية. وجد الباحثون أن الخلايا السرطانية المختلة الصيغة الصبغية تظهر حساسية متزايدة للأضرار التي تلحق بالآلية التي تتحكم في فصل الكروموسومات أثناء انقسام الخلايا (نقطة التفتيش الانقسامية).
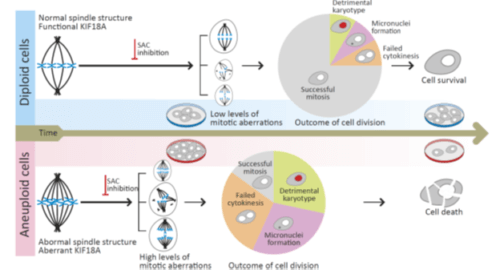
بالإضافة إلى ذلك، اكتشف الباحثون الأساس الجزيئي لزيادة حساسية الخلايا السرطانية المختلة الصيغة الصبغية. وباستخدام الأساليب الجينومية والمجهرية، راقب الباحثون فصل الكروموسومات في الخلايا المعالجة بمادة معروفة بتثبيط آلية التحكم في فصل الكروموسومات. ووجد الباحثون أنه عندما يتم تثبيط الآلية في الخلايا ذات التركيب الصبغي الطبيعي، يتوقف انقسام الخلايا. ونتيجة لذلك، تتمكن الخلايا من فصل الكروموسومات بشكل صحيح، وتنشأ مشاكل كروموسومية قليلة نسبيًا. على العكس من ذلك، عندما يتم تثبيط الآلية في الخلايا المختلة الصيغة الصبغية، يستمر انقسام الخلايا، ولكنه يكون مصحوبًا بتكوين العديد من التغيرات الصبغية التي تضعف قدرة الخلايا على الانقسام وحتى تؤدي إلى موتها.
البحث له آثار مهمة على عملية العلاج في طب السرطان الشخصي. الأدوية التي تمنع آلية فصل الكروموسومات تخضع حاليًا للتجارب السريرية، لكن من غير المعروف أي المرضى سيستجيبون للأدوية ومن لن يستجيبوا. وبمساعدة البحث، سيكون من الممكن استخدام اختلال الصيغة الصبغية كعلامة بيولوجية يمكن على أساسها تحديد المرضى الذين سيستجيبون بشكل أفضل لهذه الأدوية. وهذا هو، لأداء تكييف أدوية العلاج الكيميائي الموجودة مع الأورام ذات الخصائص الوراثية المحددة.
بخلاف ذلك، يقترح الباحثون التركيز في تطوير أدوية جديدة على مكونات محددة لآلية التحكم في فصل الكروموسومات، والتي تم تحديدها على أنها مهمة بشكل خاص للخلايا السرطانية المختلة الصبغية. تتكون آلية التحكم في فصل الكروموسومات من عدة بروتينات. يظهر البحث أن حساسية الخلايا المختلة الصيغة الصبغية تجاه الأضرار التي تلحق بالبروتينات المختلفة ليست هي نفسها، وهناك بروتينات معينة تكون أكثر تضرراً. وبالتالي، توفر الدراسة حافزًا لتطوير مثبطات محددة للبروتينات الإضافية في آلية التحكم.
"يجب التأكيد على أن البحث تم على خلايا في المزرعة وليس على مرضى السرطان، ومن أجل ترجمته إلى علاج مرضى السرطان، يجب إجراء العديد من دراسات المتابعة. ومع ذلك، فمن الواضح بالفعل في هذه المرحلة أن البحث قد يكون له العديد من العواقب الطبية". دكتور بن دافيد.
تم إجراء البحث بالتعاون مع مختبرات من خمس دول مختلفة: الدكتورة سوزانا ستورتشوفا (جامعة كايزرسلاوترن التقنية، ألمانيا)، والدكتور جيسون شتومبف (جامعة فيرمونت، الولايات المتحدة الأمريكية)، والدكتور ستيفانو سانتاجويدا (جامعة ميلانو، إيطاليا)) والدكتور تود جولوف (المعهد العريض لمعهد ماساتشوستس للتكنولوجيا وجامعة هارفارد بالولايات المتحدة الأمريكية).
المزيد عن الموضوع على موقع العلوم:
