يستخدم الباحثون كريسبر. إدخال شريحة وراثية في كروموسوم Y لدى البعوض، تؤدي إلى حدوث طفرة في كروموسوم X المجاور له، أثناء تكوين الخلايا المنوية. ونتيجة لذلك، يفقس البعوض الذكور فقط
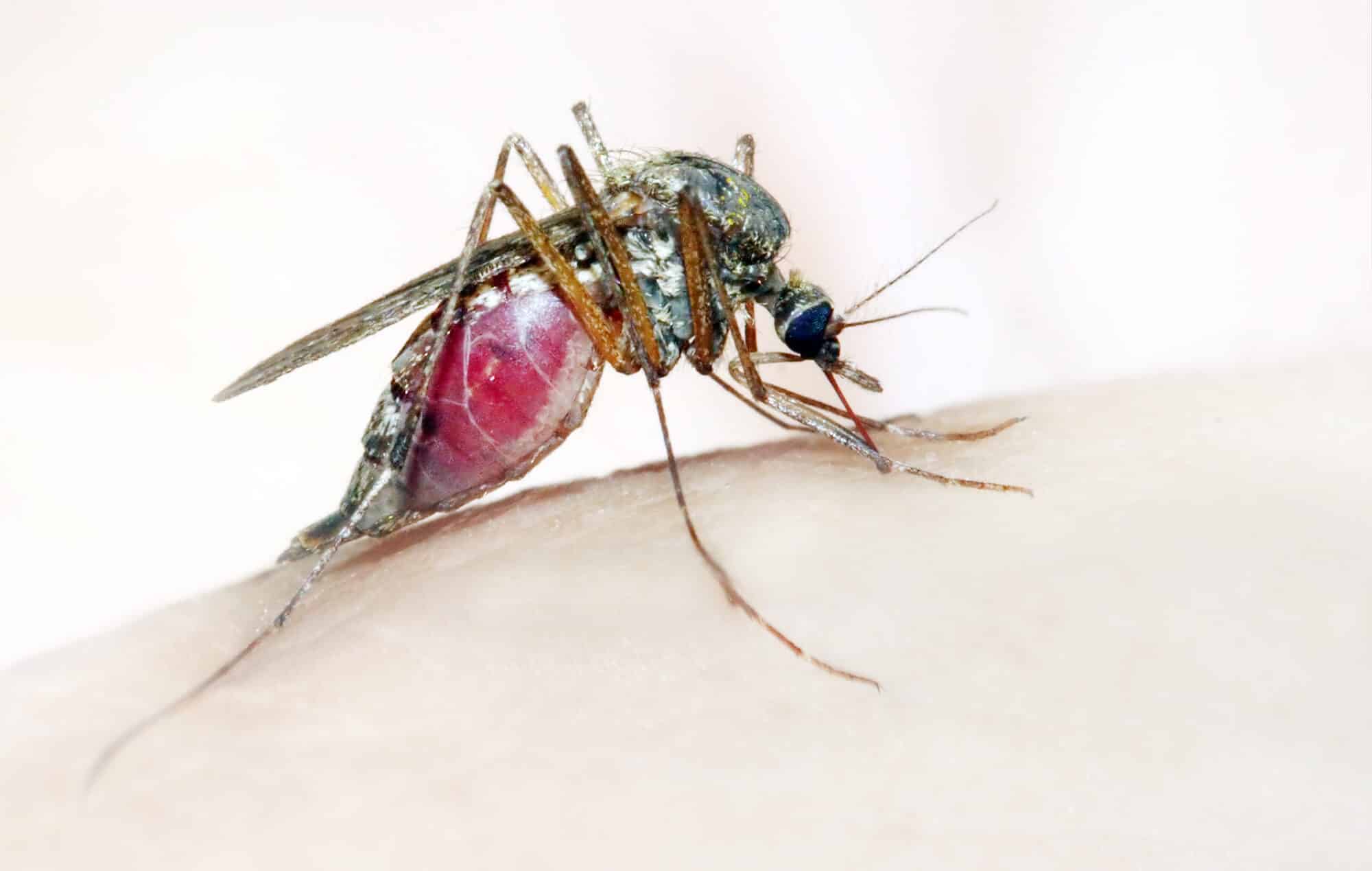
لا تزال الملاريا أو حمى المستنقعات منتشرة حتى يومنا هذا، خاصة في البلدان الحارة والفقيرة في أفريقيا وجنوب شرق آسيا. وهذا المرض يصاب به سنويا نحو 200 مليون شخص ويموت منهم نحو 400 ألف أغلبهم دون سن الخامسة. في مختبر الدكتور بابثانوس فيليبوس من قسم علم الحشرات في كلية الزراعة في الجامعة العبرية، يتم استخدام تقنية كريسبر لتحرير جينوم مجموعات بعوض الأنوفيلة وبالتالي القضاء على مجموعات البعوض التي تنقل المرض.
ما هو السؤال؟
كيف يمكن أن يتضرر البعوض الناقل لطفيليات الملاريا، عن طريق طفرة في جينوم ذكور البعوض؟
مرض الملاريا يسببه طفيل يعرف باسم Plasmodium، وتشمل دورة حياته إصابة عدة أنواع من البعوض من نوع Anopheles، وأكثرها شيوعاً الأنوفيلة الغامبية سبب المرض في شرق أفريقيا. تتغذى أنثى البعوض على دم المضيف الذي تلدغه، وفي هذه العملية تنقل الطفيليات وحيدة الخلية إلى مجرى الدم البشري، حيث تدمر خلايا الدم الحمراء وتسبب فقر الدم. بالمناسبة، الذكور لا يتغذىون على الدم وبالتالي لا يشكلون خطرا وبائيا. ولذلك يجب أن يتضمن الحل التدخل في دورة حياة الطفيلي.
لا يوجد حتى الآن لقاح مضاد للملاريا، وحتى الأدوية الموجودة التي تعطى للمسافرين إلى المناطق المتضررة من الملاريا لها آثار جانبية. علاوة على ذلك، فإن البعوض الذي يحمل الطفيل يطور مقاومة للأدوية الموجودة. إن استخدام مادة الـ دي دي تي لأغراض مكافحة الآفات، والذي كان شائعًا في الأربعينيات من القرن العشرين، أصبح غير قانوني اليوم نظرًا لأنه، باستثناء يرقات البعوض، يدمر كل حيوان ونبات في المنطقة.
وفي السنوات العشرين الماضية، ظهر حل آخر: إطلاق الذكور العقيمين إلى الطبيعة، والذين سيتزاوجون مع الإناث ويتسببون في الواقع في انخفاض كبير في عدد الجيل القادم. وهذه طريقة مكلفة، لأنه يجب تكرار الإطلاق من وقت لآخر، من أجل التنافس مع ذكور البعوض الخصبة الموجودة في البرية. بالإضافة إلى ذلك، يجب إطلاق عدد من البعوض أكبر بـ 20 مرة من البعوض الموجود بشكل طبيعي في نفس الموطن. هذا بالإضافة إلى البعوض القادم من المستنقعات القريبة والذي يستطيع اختراق الموطن.
يمتلك مختبر وراثة الحشرات بقيادة الدكتور بابثانوس فيليبوس، وهو محاضر كبير في الهندسة البيولوجية للحشرات في كلية الزراعة والأغذية والبيئة في الجامعة العبرية في رحوفوت، حلاً مبتكرًا حصل حتى على تمويل من مؤسسة العلوم الوطنية وهي الهيئة التي تشجع العلوم الأساسية في إسرائيل.
للتنافس مع ذكور البعوض الخصبة الموجودة في البرية، عليك إطلاق بعوض أكثر 100 مرة من البعوض الموجود بشكل طبيعي في نفس الموطن. هذا بالإضافة إلى البعوض القادم من المستنقعات القريبة والذي يستطيع اختراق الموطن.
يستخدم الباحثون أدوات التحرير الجيني المعتمدة على تقنية كريسبر. باستخدام هذه الطريقة، يتم إدخال شريحة وراثية في كروموسوم Y للبعوض الذي يسبب طفرة في كروموسوم X المجاور له، أثناء تكوين الخلايا المنوية (تكوين الحيوانات المنوية)، وهذا الإجراء لا يضر النسل الذكر، ولكنه يسبب التكاثر. وفاة الإناث، التي ترث كروموسوم X المطفر من والدها.إطلاق البعوض من المتوقع أن يقوم الذكور الذين خضعوا لمثل هذا التحرير الجيني بقمع أعداد البعوض في منطقة الإطلاق حتى الانقراض المحلي، دون التسبب في انقراض النوع بأكمله.

إن تطوير طريقة التحرير الجيني كريسبر أكسب الباحثين إيمانويل شاربنتييه وجنيفر داوندا جائزة نوبل في الطب وعلم وظائف الأعضاء لعام 2020. إن فكرة إدخال الجينات في المكان المحدد الذي تريد أن يكون لها فيها تأثير في النبات أو الحيوان لقد بدأ بالفعل في تغيير وجه الطب والزراعة.
يقول الدكتور فيليبوس: "تركز أبحاثنا على تطوير طرق لقمع مجموعات البعوض وحتى القضاء عليها باستخدام طرق آمنة للبيئة". "إن عدد الإناث الخصبة هو العامل الذي يحدد حجم السكان، وفي حالة الأنوفيلة هم الذين يسببون أضرارا صحية واقتصادية هائلة. وفي الوقت نفسه، نعمل على تطوير تقنية أخرى نطلق فيها ذكور البعوض البرية التي تحمل تسلسلًا جينيًا من المتوقع أن ينتشر مع مرور الوقت بين السكان ولن يتطلب الإطلاق المستمر للبعوض. وهذا ما يسمى محرك الجينات.
في الواقع، يستخدم الدكتور فيليبوس وطلابه وشركاؤه في البحث الطريقة الرئيسية التي تحدد مصطلح التطور: عملية التغيير الجيني في مجموعة من الكائنات الحية على مدى أجيال من خلال التغيرات في وتيرة ظهور الأليلات في المجموعة.

ويقول الدكتور فيليبوس أن هذا البحث لا يزال في مرحلة المختبر. "في الخطوة الأولى، نقوم بتطوير ذكور عقيمة باستخدام نفس الطريقة حتى نتمكن من مقارنة الطريقة بالطرق المستخدمة في المختبرات الأخرى التي تتعامل مع هذا الأمر حول العالم. ولكن من الجدير بالذكر أنه لم يتم إطلاق أي كائن حي تم تصميمه باستخدام تقنية كريسبر في الطبيعة حتى الآن". ويضيف أن الأمر سيستغرق وقتا طويلا حتى نصل إلى مرحلة التقديم الكامل. وفي الوقت نفسه، سيكون من الضروري وضع اللائحة التنظيمية في مجال الهندسة الوراثية، لضمان عدم سيطرة الأصناف المعدلة وراثيا على البيئة.

الحياة نفسها:
الدكتور فيليبوس، يوناني الأصل، درس في إمبيرال كوليدج في لندن. حصل على درجة ما بعد الدكتوراه في معهد كاليفورنيا للتكنولوجيا، كاليفورنيا، ومن هناك انتقل إلى جامعة بيروجيا في إيطاليا، حتى انتقل أخيرًا في عام 2018 إلى إسرائيل، متبعًا زوجته الإسرائيلية، وهي أيضًا عالمة التقى بها عندما كانا في مرحلة ما بعد الدكتوراه. الدكتوراه في معهد كاليفورنيا للتكنولوجيا. "هناك مثل يوناني يقول إذا رأيت قارباً على قمة جبل، فهذا يعني أن امرأة وضعته هناك." يمكن للمرأة أن تفعل أي شيء. هذا هو الجواب الذي يقدمه لمن يتساءل عما يفعله الباحث اليوناني في إسرائيل.
ووفقا له، فقد اختار على وجه التحديد معمل وراثة الحشرات بكلية الزراعة لأنه كان منبهرا بالانعكاسات التطبيقية المستقبلية لصالح البشرية. وفي الوقت نفسه، يقوم بالتحقيق في استخدامات نفس التكنولوجيا أيضًا ضد الحشرات الضارة بالزراعة.
المزيد عن الموضوع على موقع العلوم:
- البعوض على الرأس
- الزراعة والملاريا وغيرها من المشاكل
- طريقة تقييم دقيقة لتحرير الجينوم باستخدام تقنية كريسبر
- الهندسة الوراثية والهجينة الحيوانية والبشرية: كيف تقود الصين انقسامًا عالميًا في الأبحاث المثيرة للجدل
- يثبت فشل تجربة الأطفال المعدلين وراثيا في الصين أننا لسنا مستعدين للتحرير الجيني للأجنة البشرية
תגיות:
