علماء معهد وايزمان للعلوم فكوا رموز الآلية الجزيئية لـ "العودة إلى الوضع الطبيعي" واكتشفوا أنها تعتمد على تصنيف البروتينات لتدميرها برمز خاص يعرف باسم "SUMO"
إن التعامل مع عوامل التوتر أمر مهم ليس فقط بالنسبة لنا ولكن أيضًا لخلايانا. في ظروف الشدة الشديدة، تقوم الخلايا بتكوين تجمعات مؤقتة تسمى "حبيبات الإجهاد" تساعدها على التعامل مع الحرارة أو البرودة أو غيرها من حالات الشدة التي قد تضرها. ومع ذلك، عندما لا تتحلل هذه الحبيبات بعد زوال الخطر، فإنها يمكن أن تتراكم في المقصورة - مثل السيارات القديمة التي تملأ ساحة الخردة. ويعتقد اليوم أن هذه "القصاصات" قد تؤدي إلى أمراض تنكسية في الجهاز العصبي. علماء معهد وايزمان للعلوم، بالتعاون مع شركائهم البحثيين، تم فك رموز الآلية الجزيئية مؤخرًا والتي يتم من خلالها تحلل الحبيبات العنكبوتية في الخلايا السليمة وأظهر أن تعزيز هذه الآلية قد يمنع التنكس العصبي المميز لمرض التصلب الجانبي الضموري (ALS).
تتكون حبيبات إيكا من جزيئات الحمض النووي الريبي (RNA) والبروتينات المرتبطة بها. ومن المعروف الآن كيف تتكون هذه الحبيبات، ولكن حتى الآن لم يعرف كيف تتحلل. تعتبر حبيبات الإيكا التالفة التي لم تتحلل بشكل صحيح مرحلة أولية لتكوين مجموعات بروتينية تسمى أجسام الاشتمال وتوجد في أدمغة المصابين بمرض التصلب الجانبي الضموري والفص الجبهي وخرف الفص الصدغي وغيرها من أمراض التنكس العصبي. مجموعة البروفيسور عيران هورنشتاين من قسم علم الوراثة الجزيئية بالمعهد يبحث في عملية تحطيم هذه الحبيبات لفهم ما يحدث عندما تسوء هذه العملية.

قاد طلاب البحث هاجي مارمور-كوليت وأفياد سياني من مختبر البروفيسور هورنشتاين البحث، الذي تم إجراؤه بالتعاون مع البروفيسور تامي جيجر من جامعة تل أبيب ومع باحثين من كلية الطب بجامعة هارفارد وجامعة لوفين في بلجيكا. طور العلماء أساليب بحث جديدة سمحت لهم بعزل أجزاء صغيرة جدًا من الخلايا البشرية وتوصيف جميع البروتينات باستخدام التحليل الطيفي الشامل. وهذه هي الطريقة التي رسم بها العلماء خريطة لمحتويات الحبيبات المعروفة أيضًا وتعرفوا على حوالي مائة بروتين جديد وبنى تحتية مجهرية لم تكن معروفة حتى الآن. ولدهشتهم، اكتشفوا أنه أثناء خضوع الحبيبات للتحلل، فإنها تقوم بتجنيد العشرات من البروتينات الإضافية، التي تشارك بشكل مباشر في عمليات التحلل.
نجح العلماء في فك رموز سلسلة جديدة ومثيرة للدهشة من التفاعلات الكيميائية الحيوية لتكسير حبوب السنط، والتي تعتمد على تصنيف البروتينات للتدمير باستخدام رمز خاص يسمى "SUMO" (SUMO - اختصار لمعدلات صغيرة تشبه اليوبيكويتين). . وهكذا، كان الباحثون متحمسين لاكتشاف أن مثل هذا النشاط المحدد يلعب دورًا حيويًا وغير متوقع في عملية التحبيب.
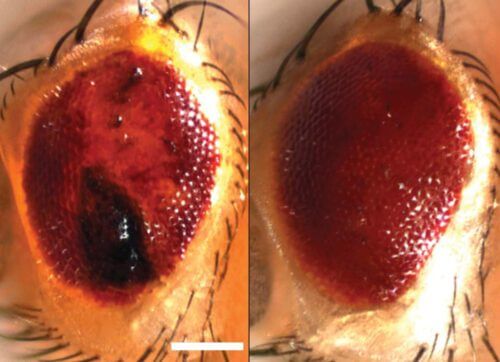
حالة مرض التصلب الجانبي الضموري
وجد العلماء أن النتائج التي توصلوا إليها كانت صالحة لأمراض الدماغ التنكسية: بعد تعريض الخلايا لبروتين سام يسبب مرض التصلب الجانبي الضموري لدى البشر، لم تتحلل حبيبات AKA بشكل صحيح ولم يتم تجنيد علامات SUMO بشكل صحيح. علاوة على ذلك، عندما طبق العلماء مصفوفة السومو على ذباب الفاكهة الذي تم تصميمه لتطوير مرض يشبه التصلب الجانبي الضموري، تمكنوا من وقف تدهور خلاياهم العصبية.
تفتح النتائج اتجاهًا بحثيًا جديدًا للآليات الكامنة وراء مرض التصلب الجانبي الضموري وغيره من أمراض التنكس العصبي. يقول البروفيسور هورنشتاين: "قد يشجع بحثنا على تطوير علاجات مستقبلية، حيث يبدو أن زيادة نشاط علامات السومو يمثل اتجاهًا جديدًا واعدًا لعلاج أمراض التنكس العصبي". يتخصص مختبر البروفيسور هورنشتاين في أبحاث التصلب الجانبي الضموري لسنوات عديدة وقد قام بتطوير علاج هو حاليًا في المرحلة الثانية من التجارب السريرية على مرضى التصلب الجانبي الضموري في معهد مونتريال للأعصاب (MNI) في كندا؛ هناك علاج آخر تم تطويره في المختبر وهو في مرحلة ما قبل السريرية. يعتمد كلا العلاجين على آليات تعتمد على الحمض النووي الريبي الميكروي (microRNA)، وهي جزيئات بيولوجية صغيرة تلعب أدوارًا تحكم مختلفة في الخلية.
ناتالي ريفكين، يهودا ماتان دانينو، د. تسفيا أولاندر، داود شيبان، نير كوهين، ريفيتال رافيد، تشين إيتان، د. بياتا توت كوهين وأستاذ جامعي. يعقوب حنا من قسم الوراثة الجزيئية بالمعهد؛ د. تالي دعدوش من قسم البنى التحتية للبحوث الكيميائية في المعهد؛ الدكتور يوسف عدي من قسم البنى التحتية لأبحاث علوم الحياة في المعهد؛ الدكتور يفعات للرخام من قسم علم المناعة بالمعهد. د. نانسي قادرشا، سارة هوفمان، كلير ريجز، د. ويوك إم. أديباني، البروفيسور بول أندرسون والبروفيسور بافيل إيفانوف من كلية الطب بجامعة هارفارد؛ نعمة كنافو من جامعة تل أبيب؛ دكتور توماس سي. موينز والبروفيسور لودو فان دن بوش من جامعة لوفين في بلجيكا؛ والدكتور أدريان هيجينبوتوم والدكتور جون كوبر نوك من جامعة شيفيلد.
المزيد عن هذا الموضوع على موقع العلوم:
