طباعة الأعضاء البديلة بطريقة تسمح بزراعتها في جسم الإنسان ودمجها في عملياته

في سن العاشرة، واجه لوك خيارين لا يضطر الأطفال عادةً للاختيار بينهما: زراعة الكلى، أو حياة قصيرة مع زيارات متكررة إلى المستشفى لعلاج كليتيه الفاشلتين. اختار والداه الخيار الثالث: إجراء عملية جراحية غير عادية وتجريبية. جمع البروفيسور أنتوني أتلا من جامعة ويك فورست خلايا من مثانة لوك وقام بزراعتها في المختبر بصبر وحب. وقام بالتعاون مع فريقه البحثي بإنشاء سقالة لهم: كرة من البوليمر الاصطناعي على شكل نفطة جديدة. وقام الباحثون بتبطين المثانة الاصطناعية بخلايا عضلية من الخارج وخلايا تغطي المثانة الطبيعية من الداخل. لقد راقبوا العضو الطبيعي الاصطناعي لأسابيع أثناء وجوده في مفاعل حيوي في المختبر، وعلموا أن الخلايا تتكاثر وتبث حياة حقيقية فيه. وأخيراً قاموا بزرعه في جسد الشاب لوك[1].
استعاد الصبي حياته.
واليوم، لا يزال لوك يتمتع بصحة جيدة. كان العلاج الثوري في ذلك الوقت - إنشاء عضو بديل كامل - ناجحًا تمامًا[2].
ماذا لو تمكنا من فعل ذلك بأعضاء أخرى في الجسم؟
الجواب - على الأقل إجابة واحدة محتملة - قدمها لي أستاذ الطب المحترم قبل عقد من الزمن. وتنبأ لي نفس الأستاذ أن اليوم الذي سنتمكن فيه من استبدال أعضاء الجسم، عضوًا بعد عضو، ليس بعيدًا.
"هل أصبح القلب سيئًا؟" فقال: سنستبدله. هل انهارت الكلى؟ هم أيضا. هل أنت غير راض عن حالة بشرتك؟ وسيكون من الممكن علاجه أيضًا."
وستكون نتيجة هذا الوضع، في رأيه، وقف الشيخوخة من كافة النواحي العملية. يمكننا أن نتجادل حول التفاصيل الصغيرة في الرؤية، لكن من الواضح أنه عندما نتمكن من استبدال كل نسيج في الجسم، فإن الكثير من الأمراض التي تزعجنا اليوم ستظهر لنا في المستقبل على أنها تافهة يمكن علاجها. ربما تكون تفاهات غير سارة، ولكن مثلما نذهب إلى طبيب الأسنان اليوم ونرغب في المعاناة من أجل الصحة، كذلك في المستقبل سنكون أيضًا على استعداد للذهاب إلى "مهندس الأنسجة" في المستشفى لتمديد مدة العلاج. حياتنا الصحية في عقد أو عقدين.
حسنًا، الرؤية شيء جيد، لكنك لا تدفع بها في متجر البقالة. ومن ثم فإن السؤال الذي يطرح نفسه هو إلى أي مدى يمكننا حاليًا إيجاد بدائل للأنسجة والأعضاء، وما هي التحديات الكبرى في هذا المجال - ومتى سنصل حقًا إلى الأرض الموعودة بصحة لا نهاية لها.
لنبدأ بالبدائل الأقل إثارة للإعجاب للوهلة الأولى: الأعضاء البديلة غير الحية.
كان ريكارد نورماك على وشك منتصف العمر عندما فقد ذراعه في حادث عمل. حصل على طرف اصطناعي - ذراع صناعية تقليدية. تلك الذراع، التي كانت تذكرته إلى عالم الأعضاء البديلة، كانت مربوطة بمنطقة الجذع بكم كان من المفترض أن يكون مخصصًا له.
وهذا، على الأقل، هو الوعد. الحقيقة أقل متعة: من الصعب إيجاد طريقة مناسبة لربط الأعضاء الصناعية بالجسم، ولم يتمكن نورماك من التعود على الطرف الاصطناعي الجديد[3]. ولم يقم بتنشيطه بشكل جيد. لقد كانت، بكل بساطة، طرفًا ميتًا.
وفي هذا الصدد، تشبه قصة نورماك تجارب الكثيرين الذين يضطرون إلى استبدال أذرعهم البيولوجية الأصلية بعضو بلاستيكي معدني. معظم الأطراف الاصطناعية للذراع اليوم بسيطة بطبيعتها. أبسطها يشبه الخطاف الممدود الذي يمكن إغلاقه عن طريق تحريك المرفق أو الكتف بطريقة تؤدي إلى تمدد الأربطة في الطرف الاصطناعي. أما الأنواع الأكثر تطورًا فهي قادرة على استقبال الإشارات الكهربائية التي تأتي عادةً من الأعصاب الموجودة في منطقة الصدر، وترجمة هذه الإشارات العصبية لتشغيل المفاصل الاصطناعية و"العضلات". وتعاني هذه الأجهزة أيضًا من نفس المشاكل: صعوبة ارتدائها على الجسم، وصعوبة التحكم بها، وصعوبة نقل التغذية الراجعة إلى الأعصاب، بحيث يستعيد المستخدم الإحساس بيده وأصابعه.
بعد بعض المداولات، قرر نورماك الحصول على نوع جديد من الأطراف الاصطناعية: طرف يصبح جزءًا من الجسم لجميع المقاصد والأغراض. تم ربط الطرف الاصطناعي الآلي بجسده من خلال عملية التكامل العظمي: حيث تم إدخال زرعة معدنية - مصنوعة عادة من التيتانيوم - في العظم، وتم تشجيع الخلايا العظمية على الهجرة إلى المعدن المثقب وملئه بأنسجة عظمية صحية. . وبعبارة أخرى، فإن العظم والمعدن - الحي وغير الحي - متكاملان معًا بشكل طبيعي[4].
لم يتم دمج الطرف الاصطناعي الذي تلقاه نورماك مع العظام فحسب، بل أيضًا مع الأعصاب والعضلات. وتمت مطابقة الأقطاب الكهربائية الذكية مع الأعصاب المناسبة، وترجمت الخوارزميات المتطورة الرسائل إلى تعليمات يتم إرسالها إلى الذراع الروبوتية والكف والأصابع. تدفقت المعلومات في كلا الاتجاهين: عندما لمست الأصابع الروبوتية التفاحة، على سبيل المثال، تم إرسال إشارة كهربائية على الفور إلى أجهزة الاستشعار الموجودة حول الأعصاب. ترسل الأعصاب المعلومات إلى الدماغ، لذلك يستطيع نورماك أيضًا الاستمتاع بحاسة اللمس الحقيقية[5].
"عادةً ما أقول إنه مع الأكمام الاصطناعية التقليدية، فإنك ترتدي الطرف الاصطناعي - فهو جهاز طبي. ولكن مع التكامل العظمي، يصبح الجهاز الطبي جزءًا منك. لا تشعر وكأنك ترتدي الطرف الاصطناعي. بل هي جزء منك." قال.
تعلمنا قصة ريكارد نورماك عدة دروس. أولا، يوضح أننا لا نستطيع التعامل تلقائيا مع الأعضاء البديلة كما لو كانت بيولوجية بحتة. على غرار ورقة البوليمر الاصطناعية التي زرع فيها أنتوني أتلا خلايا مثانة لوك، أصبحت ذراع نورماك أيضًا مزيجًا من المواد البيولوجية إلى جانب المواد التي لا توجد بشكل طبيعي في الجسم. نحن نخجل تلقائيًا من مثل هذه التركيبات - التي يراها الكثيرون وحشية وغير طبيعية - ولكن من المستحيل إنكار الفوائد الهائلة التي تجلبها لأصحابها.
الدرس المهم الثاني هو أن الأطراف الاصطناعية لا يجب أن تستمر في الظهور مثل الطرف الأصلي. وتكشف مقاطع الفيديو التي تظهر طرف نورماك الاصطناعي نقطة اتصاله بالذراع، وهو مشهد يثير الإيلاج. ولكن مرة أخرى، هنا أيضًا، فإن الاستعداد لتجاهل الشكل الأصلي للطرف يمكن أن يساعد متلقي الطرف الاصطناعي.
ونرى هنا استمرارا لحركة بدأت في أواخر السبعينيات، عندما تعرض فان فيليبس -الطالب الشاب- لحادث انتهى ببتر ساقه من تحت الركبة. كانت الأطراف الاصطناعية التي تم تركيبها عليه غير مرضية لدرجة أنه تحول إلى الهندسة الطبية الحيوية وطور أطرافًا اصطناعية كانت أكثر فائدة من التمثيلية. كان هذا هو الوقت الذي قفزت فيه هندسة المواد إلى الأمام، وبدأت المواد القوية والخفيفة من صناعة الطيران تجد طريقها إلى الأطراف الاصطناعية أيضًا. قامت شركة Philips بتطوير Flex-Foot، الذي يسمح نسله الروحي للعدائين في الألعاب البارالمبية بالوصول إلى سرعات تنافس العدائين غير المعاقين[6]. لا تشبه هذه الأطراف الاصطناعية الأرجل، لكنها تمنح المستخدم قوى خارقة خفيفة.
في أيامنا هذه، يبدو أن الناس أقل خجلًا من أعضائهم البديلة. يمكنك العثور على صور عبر الإنترنت لأذرع وأرجل صناعية مرصعة بالماس ذات لون وردي فاتح ومخالب ولفيرين، والكثير من اختراعات السايبربانك الأخرى. لقد بدأ المصممون للتو في استكشاف عوالم الجمال المحتمل وأشكال الأعضاء البديلة، وسيكون من الرائع أن نرى إلى أين سيأخذوننا.
هذا الدرس الثاني له أيضًا معنى مهم بالنسبة للأعضاء الداخلية: ليس علينا إعادة إنشائها تمامًا كما كانت في الأصل.
خذ على سبيل المثال البنكرياس. هذا العضو المعقد قادر على استشعار مستويات الجلوكوز - السكر - في الدم، ويفرز الأنسولين الذي من شأنه أن يخفض مستوى السكر في الدم. لقد عمل مهندسو الطب الحيوي لسنوات عديدة على إنشاء بنكرياس صناعي يمكنه أداء كل هذه المهام. في الواقع، ما زالوا يحاولون. لكن ذلك ممكن أيضًا بطريقة أخرى: بنكرياس صناعي معياري، أي بنكرياس مقسم إلى أجزاء مختلفة. يتم تثبيت جهاز استشعار الجلوكوز على الجلد في جميع الأوقات، ويفحص مستويات السكر في الدم. يتم نقل المعلومات إلى الذكاء الاصطناعي الذي يقرر ما إذا كان حقن الأنسولين ضروريًا ويحدد الجرعات المطلوبة. وأخيرًا وليس آخرًا، تقوم المضخة بضخ الأنسولين إلى الجسم من خلال إبرة صغيرة.
ويقع كل جزء من هذه الأجزاء في مكان مختلف من الجسم. هذا ليس "البنكرياس" كما نعرفه، ولكن عندما يعملان معًا، فإنهما يحلان محل البنكرياس البيولوجي. الهدف النهائي هو الأهم وليس طريقة تحقيقه.
كما يفتح لنا هذا الدرس نافذة على تصورات غريبة ورائعة عن مستقبل الأعضاء البديلة. ربما، بدلاً من قلب واحد فقط، يمكننا وضع عدة مضخات صناعية في عدة أماكن في الجسم، والتي ستقوم معًا بنفس وظيفة القلب وتدوير الدم في جميع أنحاء الجسم؟ ربما الحل للكبد البديل ليس كبدًا بيولوجيًا واحدًا، بل سلسلة من المرشحات التي تعمل على تحييد السموم وتفكيك الملوثات؟
ربما. ربما لا. من المهم أن نفهم أنه في مجال هندسة الأنسجة والأعضاء، لا يتعين علينا أن نقتصر على "المنتج الحالي".
الدرس الثالث من قصة نورماك هو أن تقنيات اليوم قد وصلت إلى مستوى يمكنها من التفاعل مع الدماغ والأعصاب. ولهذا انعكاسات كبيرة على المستقبل، وهو ما سنتطرق إليه في الجزء الأخير من المقال. وفي غضون ذلك، سوف نعود إلى أرض الواقع ونفحص نوعًا آخر من بدائل الأعضاء: البدائل البيولوجية.
دعونا نتحدث الأرقام للحظة. وفي الولايات المتحدة وحدها، ينتظر حاليًا 106,075 شخصًا إجراء عملية زرع الأعضاء. وبعضهم لن يحصل أبداً على الأعضاء التي يحتاجها، لأن المتبرعين الأحياء يقدمون فقط 6,000 عضو سنوياً في المتوسط. يموت في المتوسط 17 شخصًا يوميًا أثناء انتظار عملية زرع الأعضاء. كل تسع دقائق، يتم إضافة شخص جديد إلى قائمة الانتظار. باختصار، الإحصائيات ليست في صالح أولئك الذين ينتظرون الحصول على عضو من الحيوان.
توجد حاليًا ثلاث طرق رئيسية لإنشاء أعضاء بديلة: إزالة الخلايا، وإنشاء الأعضاء العضوية، والطباعة ثلاثية الأبعاد. كل واحد منهم لديه مزاياه وعيوبه، ولكن هناك شيء واحد مشترك بينهم جميعًا: لا يزال لديهم مجال كبير للتحسين.
لنبدأ مع ديسيلولاريزيشن.
نحن نميل إلى الاعتقاد بأن الجسم يتكون من خلايا - وهذا صحيح، ولكن جزئيا. في الواقع، تفرز الخلايا حول نفسها نسيجًا يُعرف باسم "المصفوفة خارج الخلية"، وتستقر بداخله. تدعمها المصفوفة، وتثبتها، بل وتتواصل معها وتعطيها التعليمات الكيميائية التي تفرزها الخلايا الأخرى. بدون المصفوفة خارج الخلية، لن تتمكن الخلايا في الجسم من العمل أو البقاء على قيد الحياة.
تعتمد طرق إزالة الخلايا - إزالة الخلايا - على المصفوفة خارج الخلية كأساس للنسيج. في الخطوة الأولى، يتم غسل الأنسجة وتنظيفها من جميع الخلايا. وما يتبقى هو المصفوفة النظيفة: وهي بنية تشبه العضو الأصلي، ولكنها خالية من اللون والحياة. السبب وراء أهمية هذا الهيكل الفارغ هو أنه يحتوي على جميع البروتينات وعوامل النمو - جميع التعليمات الكيميائية - التي يمكن للخلايا الجديدة الاعتماد عليها لإعادة ملء الأنسجة. ليس هذا فحسب، بل يتم تشكيله أيضًا بالطريقة الصحيحة تمامًا: القلب أو الكبد أو العظام أو أي عضو آخر.
تُستخدم طريقة إزالة الخلايا حاليًا في بعض الحالات، مثل إعادة بناء الثدي. يتم زرع المصفوفات التي يتم تنظيفها من خلاياها في الثدي، وتجذب الخلايا التي تتكون منها الأوعية الدموية في الجسم بنجاح كبير، بحيث تخترق المصفوفة وتملأها بالأوعية الدموية. بعد ذلك، يتم أيضًا حقن الخلايا التي تنقسم وتتطور إلى خلايا دهنية في المصفوفات[7].
لسوء الحظ، ليس لدي علم بحالة استبدال عضو كامل ومعقد في شخص ما بمصفوفة منزوعة الخلايا. وفي واحدة من أكثر الدراسات تقدما على الخنازير، حصلوا على قلب خنزير آخر تم تنظيف خلاياه. وتمكنوا من البقاء على قيد الحياة لمدة ثلاثة أيام، قبل أن يتم حصاد القلوب لفحصها عن كثب تحت عدسة المجهر. من الواضح بالنسبة للبشر أننا مهتمون بالنجاح على المدى الطويل[8].
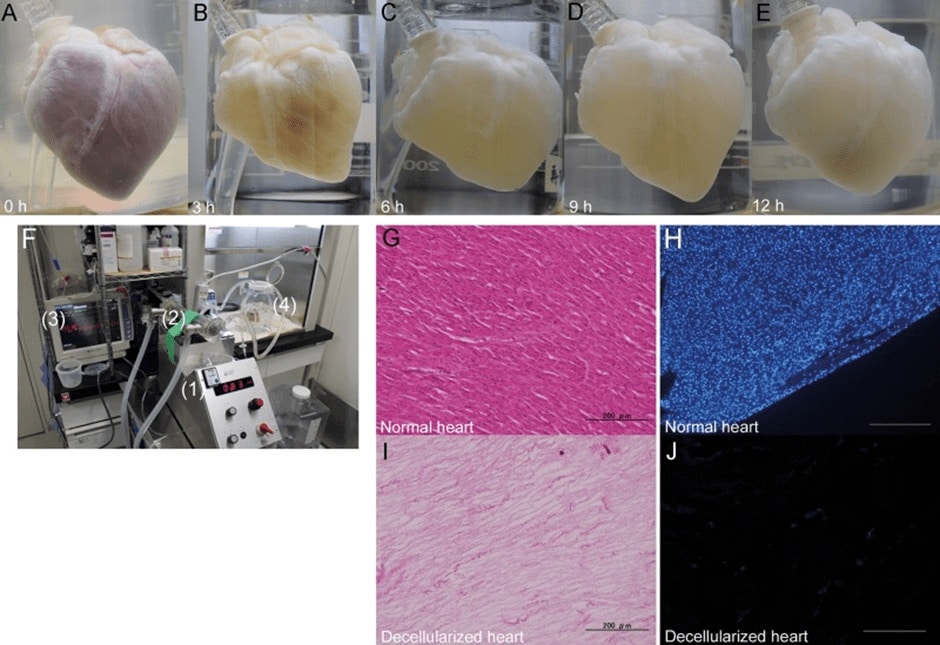
مشكلة أخرى تتعلق بنزع الخلايا هي أن الطريقة لا تزال تتطلب الاعتماد على الأعضاء التي تأتي من البشر. من الممكن نظريًا استخدام مصفوفات ذات أصل حيواني، لكن من الواضح أنها لن تكون ناجحة مثل المصفوفات البشرية.
عضوي
في منتصف عام 2021، ظهرت أخبار غريبة في الصحافة الدولية: "أدمغة صغيرة في المختبر قامت بتنمية أزواج من العيون الخاصة بها". إنها واحدة من تلك الحكايات التي تتوقع رؤيتها في الخيال العلمي، لكنها معاصرة بالتأكيد. تلك "الأدمغة الصغيرة" هي الأعضاء العضوية.
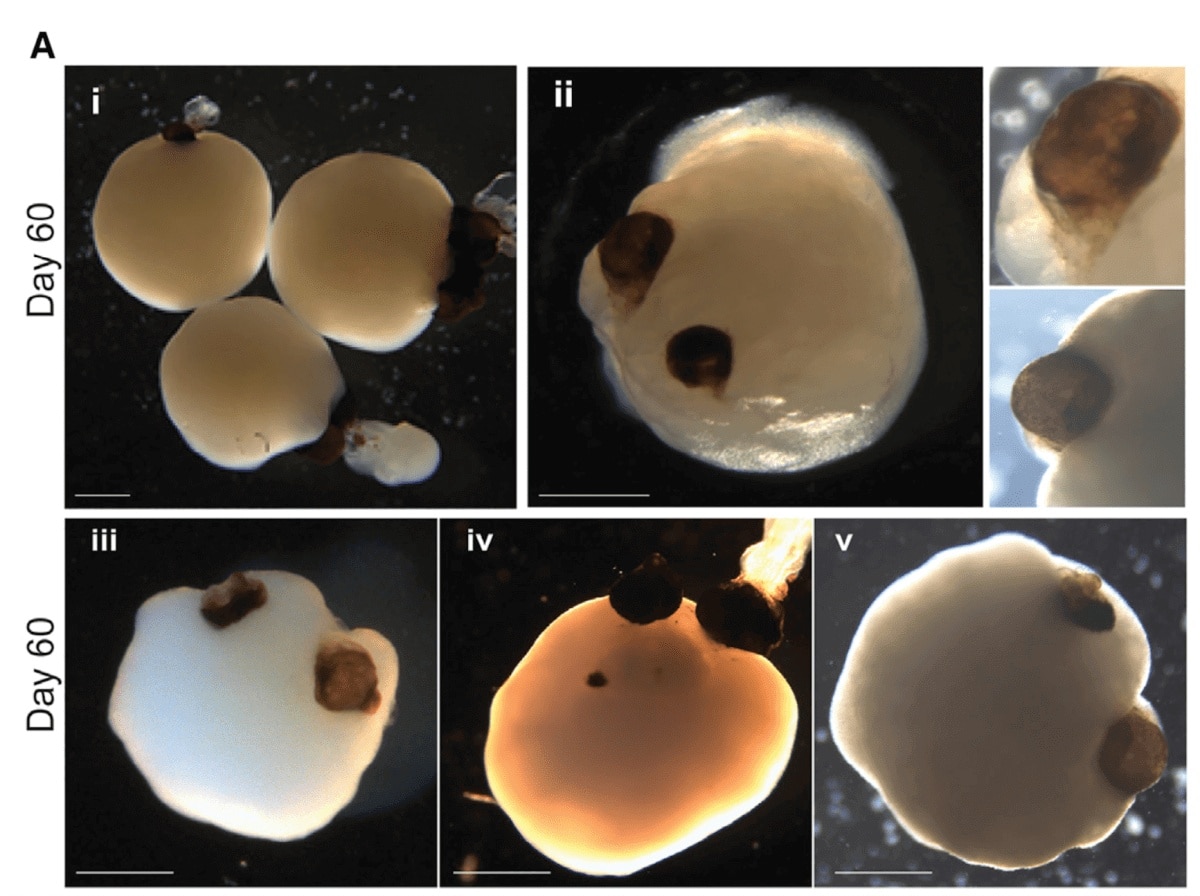
لشرح مصدر الكائنات العضوية، نحتاج أولاً إلى معرفة الخلايا الجذعية: نوع من الخلايا البدائية القادرة على التمايز إلى أنواع مختلفة من خلايا الجسم. ويتكون الجنين البشري، في مراحل نموه الأولى، من هذه الخلايا الجذعية. تتلقى هذه الخلايا تعليمات مختلفة في جسم الجنين، وبالتالي تتمايز إلى أنسجة مختلفة: أنسجة المخ، وأنسجة الكبد، وأنسجة العظام وكل ما تبقى.
ماذا سيحدث إذا أخذنا الخلايا الجذعية ووضعناها في طبق بتري وأعطيناها تعليمات لتكوين نسيج معين؟ لقد أنتجوا "عضويًا" - وهو نسيج صغير يحاكي أنسجة وأعضاء جسم الإنسان.
وبنفس المعرفة عن الأدمغة الصغيرة التي أنتجت عيونًا جديدة، تلقت الأعضاء تعليمات من الباحثين للتمييز وإنشاء الخلايا العصبية وهياكل الدماغ. ومن الطبيعي أن يستمر النمو في تكوين الأعصاب المؤدية إلى العينين، وتظهر الكؤوس البصرية - وهي الهياكل الأساسية التي من المفترض أن تنمو فيها الشبكية - خلال ثلاثين يومًا وتنضج بحلول اليوم الخمسين. وهذا أيضًا هو الطول المقدر لتطور مماثل في الجنين البشري. كما واصلت الكائنات العضوية تطوير العدسات وأنسجة القرنية[10].
هل يعني هذا أننا سنكون قادرين قريبًا على زرع عيون بيولوجية، والتي سيتم تطويرها على عضوي؟
لسوء الحظ، لا يبدو أن هذا هو الحال. العضو العضوي هو مجرد تقليد للعضو الأصلي. ورغم أنه مطابق في بنيته الداخلية لبنية العضو الحقيقي، إلا أنه لا يصلح للزراعة أو الارتباط بجسم الإنسان. كما أن هناك دائمًا الخوف من خروج الخلايا الجذعية عن نطاق السيطرة في الجسم المزروع، وينتج عنها ورم سرطاني قاتل. ولهذه الأسباب، لم يتم بعد استخدام الأعضاء العضوية لتحل محل الأعضاء داخل الجسم. الاستخدام الأكثر إثارة للاهتمام لها هو على وجه التحديد استبدال الأعضاء خارج الجسم: يقوم الباحثون باختبار مجموعة متنوعة من المواد العلاجية عليها، مع افتراض أنه إذا كانت هذه المواد ضارة بالعضويات، فإنها ستسبب أيضًا ضررًا للعضو الحقيقي الموجود بالداخل. الجسم.
هذا يعني أنه يتم استخدام المواد العضوية بالتأكيد. وباعتبارها أعضاء بديلة خارج الجسم، فإنها تساعد في تسريع وتيرة تقدم العلوم الطبية. ولكن في المجال السريري، لسوء الحظ، لا يوجد حتى الآن أي تقدم حقيقي.
طباعة الأنسجة
وهكذا وصلنا أخيرًا إلى الطريقة الأكثر واعدة وإثارة للاهتمام - أو على الأقل الطريقة التي تحظى بالعناوين الأكبر والأكثر تكرارًا في الصحف. هذه بالطبع طباعة أنسجة ثلاثية الأبعاد.
تبدأ عملية الطباعة ثلاثية الأبعاد عادةً بحصد خلايا المريض نفسه. يقوم الأطباء بإجراء خزعة صغيرة باستخدام إبرة، أو جراحة طفيفة التوغل. كل هذا من أجل الحصول على قطعة صغيرة من الأنسجة، يمكن إزالة الخلايا منها ونموها خارج الجسم. تقضي الخلايا الأيام والأسابيع التالية في المفاعلات الحيوية، حيث تتمتع ببيئة مشابهة لبيئة الجسم، بما في ذلك درجة الحرارة ومستوى الأوكسجين والغذاء - وحتى دورات النهار والليل والنشاط البدني، في بعض الدراسات.
هناك العديد من طرق الطباعة المختلفة، ولكن إحدى أكثر الطرق شيوعًا هي الطريقة التي تتم فيها طباعة الخلايا مباشرة مع المصفوفة التي سيتم بناء الأنسجة منها. عندما يكون هناك ما يكفي من الخلايا في المفاعلات الحيوية، يتم خلطها مع مادة الطباعة - والتي هي في الأساس نسخة أولية من المصفوفة خارج الخلية. ويتم إثراء تلك المصفوفة مسبقًا بعوامل النمو -أي التعليمات الكيميائية- التي تساعد الخلايا على فهم ما يجب عليها فعله في تلك المنطقة. غالبًا ما تتكون المصفوفة القابلة للطباعة من مواد مثل الجيلاتين والكولاجين، والتي لا تضر الجسم أو الخلايا.
يتم نقل الخلايا والحبر الحيوي إلى طابعة ثلاثية الأبعاد، والتي تقوم بحقنها في المناطق الصحيحة. إذا كنت ترغب في إنشاء نسيج معقد - على سبيل المثال، قلب - فسيكون هناك العديد من رؤوس الطباعة، كل منها سيطبع خلايا مختلفة بمصفوفة مختلفة قليلاً لكل نوع من الخلايا. مثلما تستطيع الطابعة العادية الطباعة بعدة ألوان باستخدام عدة رؤوس طباعة أو عدة خراطيش ألوان مختلفة، كذلك تقوم الطابعة ثلاثية الأبعاد بطباعة أنواع مختلفة من الأنسجة، كل منها في المكان المناسب في العضو.
يجب ألا تستغرق عملية الطباعة بأكملها أكثر من بضع ساعات، ويجب أن يكون الهيكل النهائي مشابهًا جدًا لهيكل العضو المطلوب. ومن الناحية النظرية، يمكن تعديل الحجم والشكل، اعتمادًا على المعلومات التي تأتي من الأشعة السينية ومسح العضو الأصلي للمريض.
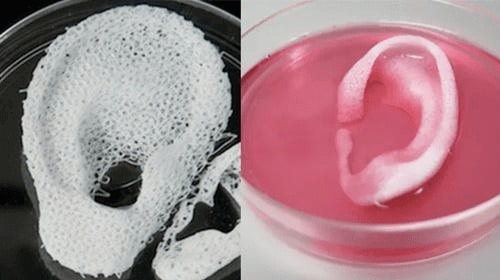
تبقى مشكلة واحدة فقط: يبدأ تدمير العضو المثير للإعجاب الذي تمت طباعته بالكامل أثناء عملية الطباعة. والسبب هو أن الخلايا تحتاج إلى الأكسجين والمواد المغذية، ولا يمكن لهذه العناصر أن تتخلل الأنسجة الكثيفة بسهولة. ولذلك، هناك حاجة للأوعية الدموية التي تشبع الأنسجة بالأكسجين. من المفترض أن تقوم الطابعات الأكثر تقدمًا بطباعة الأوعية الدموية أيضًا، لكنها لا تزال لا تعمل بسهولة أو بشكل جيد، ومن الضروري توصيلها بالأوعية الدموية الموجودة وتدفق الأكسجين بشكل نشط من خلالها. وهذا يعني أنه بمجرد وصول الأنسجة المطبوعة إلى سمك معين، تتوقف الخلايا الموجودة في عمقها عن تلقي الأكسجين - وتبدأ في الموت.
ماذا تفعلون؟ عض الشفاه وزرعها. يحاولون توصيل أكبر قدر ممكن من الأكسجين إلى الخلايا العميقة في الأنسجة لإبقائها على قيد الحياة، وزرع الأنسجة في أسرع وقت ممكن للسماح للجسم بالقيام بما يعرف كيف يفعله. الأمل هو أنه بعد عملية الزرع، سيتم إرسال الأوعية الدموية الموجودة حول المنطقة إلى الأنسجة الجديدة وتدفق الأكسجين والدم الجديد إليه. التأكيد على "الأمل"، فهو تحدٍ لم يُحل بعد.
وفي كلتا الحالتين، بعد الزرع، تبدأ المصفوفة الاصطناعية في التفكك والتفكك، تمامًا كما نريدها. لقد قامت بعملها، وزودت الخلايا بموطئ قدم والتعليمات الأولية التي تحتاجها للبقاء على قيد الحياة - والآن يتم استبدالها ببطء بمصفوفة جديدة تفرزها الخلايا بنفسها.
هذه باختصار هي عملية طباعة الأنسجة ثلاثية الأبعاد. يعد هذا إجراءً مستقبليًا تقريبًا، وقد أثبت نفسه بالفعل في العديد من الدراسات - لكنه لم يدخل الممارسة الطبية بعد. إنها لا تتقدم بعيدًا بدرجة كافية حتى الآن. الهياكل التي تخلقها ليست مستقرة بما فيه الكفاية، والخلايا الموجودة في أعماق الأنسجة تعاني من نقص الأكسجين والغذاء، وإذا كنا صادقين - فهي أيضًا باهظة الثمن. من الناحية المثالية، يتم استخدام الخلايا التي تأتي من جسم المريض نفسه، وتستغرق العملية الكاملة اللازمة لإنتاجها وزراعتها وزرعها باستخدام الطابعة، الكثير من الوقت والرعاية المخصصة.
لقد اعتدت الحديث عن الطرق المختلفة المقبولة اليوم في مجال هندسة الأنسجة، كما اعتدت أيضًا على الإجابة التي تطرح عليّ على الفور: فلماذا لا نحاول؟
نعم، لا تزال الطابعات ثلاثية الأبعاد غير فعالة جدًا في طباعة الأنسجة، ولكن لماذا لا نستخدمها لطباعة كلية أساسية وزرعها في الجسم والأمل في الأفضل؟ لماذا لا نأخذ عضويات تحتوي على أدمغة صغيرة ونفككها ونزرعها في أدمغة مرضى الزهايمر والشلل الرعاش، بحيث تقوم الخلايا العصبية التي تحتويها باستعادة الهياكل الدماغية المفقودة وتحل محل الخلايا الميتة؟ لماذا لا نقوم بإزالة الخلايا من السقالات التي تأتي من الحيوانات، ونحاول فقط؟
حصلنا على إجابة السؤال في العقد الأخير، عندما أصبح جراح إيطالي يدعى باولو ماتشياريني "أحد أشهر الأطباء في العالم"، بحسب ما نقلته هيئة الإذاعة البريطانية "بي بي سي". لقد صعد إلى الشهرة بفضل إجراء جديد طوره لاستبدال القصبة الهوائية - القصبة الهوائية - بأنسجة تم إفراغها من الخلايا وملؤها بالخلايا الجذعية. وعلى مدار ثلاث سنوات، أجرى العملية على تسعة مرضى فقدوا الأمل في عيش حياة صحية دون مساعدة وثيقة من جهاز التنفس الصناعي. تمت تغطية العمليات الجراحية على نطاق واسع وبتعاطف من قبل وسائل الإعلام، لكن النتائج لم ترق إلى مستوى الضجيج. ومن بين التسعة الذين تم زرعهم، توفي سبعة في السنوات الثلاث التي تلت عملية الزرع، ولم ينجو واحد إلا بعد إزالة القصبة الهوائية الاصطناعية المزروعة في حلقه.[11].
وبالعودة إلى الوراء، تبين أن التجارب التي أجراها ماكياريني كانت ملوثة بالإهمال، وأن الرجل طور علاقة حب مع المجتمع العلمي ووسائل الإعلام، مما سمح له بالمبالغة بالأكاذيب حول النتائج الإيجابية للتجارب. والتحليلات. بالمناسبة، الحب اللفظي، لأن الجراح أيضًا جعل المراسل يقع في حبه، وكذب عليها بأنه مطلق، ووعدها بحفل زفاف مرصع بالنجوم، يتزوج فيه البابا نفسه من الاثنين وإلتون جون. غن لهم.
يمكن استخلاص عدد من الاستنتاجات من الحلقة. على سبيل المثال، لا تكذب في العلم. الاستنتاج الآخر الذي يعرفه العلماء جيدًا هو أن كل مجال علمي أكثر تعقيدًا وتعقيدًا مما يبدو من الخارج، وأن هناك طرقًا للفشل أكثر بكثير من النجاح. وهذا ينطبق بشكل خاص في الطب.
الاستنتاج الثالث هو أن كل تجربة في الطب لها عواقب متوالية، حتى على العقلية العامة وفي أوساط المجتمع العلمي. في أعقاب فضيحة ماكياريني، تعرض المجتمع العلمي بأكمله لهجوم شديد التشكيك حول عمليات زرع القصبة الهوائية. عندما شرع الدكتور إريك غاندن في محاولة إنقاذ حياة امرأة عن طريق استبدال قصبتها الهوائية بمتبرع، حذره زملاؤه من مغبة محاولة الدخول إلى حقل الألغام هذا. كان يعتقد وظيفته -
"لقد أصبح الأمر غير ضروري، لذلك قمت بإغلاق المختبر بشكل أساسي. لا يمكنك تبرير إجراء عملية جراحية تجريبية عندما ترى شيئاً آخر يبدو مثالياً. لذا فأنت تفهم، واو، أنهم لا يحتاجون إليك."
في النهاية، قررت غاندين إجراء الإجراء الطبي، حيث قامت بزراعة جزء من القصبة الهوائية من متبرع في امرأة لم تعد قادرة على التعايش مع القصبة الهوائية المتضررة التي أهديت لها. لقد مرت العملية الجراحية بسلام، واليوم استعادت حياتها. ولكن من المحتمل تماماً أنه لولا ممارسة ماكياريني - التي أجرت بالفعل تجارب غير مسؤولة على ظهور المرضى - لكان بإمكانها هي وآخرون الاستمتاع بالتنفس الطبيعي في وقت أبكر بكثير. في الطب، كما في العلوم، لا توجد طرق مختصرة.
كل هذا لا يعني عدم الحاجة إلى تجارب جريئة أو تطوير تقنيات مبتكرة وغير عادية. ولكن يجب على المرء دائمًا أن يحافظ على التواضع ويفهم أن معظم المخفي ظاهر، وأن أي محاولة للقفز في المياه العميقة ستؤدي دائمًا إلى الغرق. وفي أسوأ الحالات، لن تكون النتيجة وفاة شخص واحد، بل أيضًا إلحاق الضرر بالحقل بأكمله على مدار سنوات عديدة. سيؤدي هذا الضرر في النهاية إلى تأخير الوقت اللازم حتى يتمكن المرضى من تلقي الأنسجة التي سيتم استخراجها وزرعها بطرق أكثر أمانًا.
في عام 1908، تمت أول محاولة لزراعة رأس كامل: تم نقل رأس كلب واحد إلى عنق كلب آخر. فشلت التجربة ومات الكلبان، لكن تلك كانت البداية فقط. استمرت التكنولوجيا في التطور، وفي السبعينيات تمكن روبرت وايت من إجراء أول عملية زرع رأس لدى القردة. وتمكن القرد الذي نقل رأسه إلى جسد آخر من البقاء على قيد الحياة لمدة ثمانية أيام، مع قدرته على تحريك عضلات الوجه، وتمتع بحاسة الشم والتذوق والسمع. كما أجريت تجارب مماثلة على الفئران والجرذان، وفي السنوات الأخيرة أيضًا على الأجسام البشرية.
يوجد حاليًا جراحون يعدون بأنهم سيقومون في العقد القادم بإجراء عملية استبدال كاملة للرأس. عندما يحدث ذلك، كل شيء سوف يتغير. يمكننا عملياً أن ننقل النفوس من جسد إلى جسد. وطالما أن أي شخص لديه ما يكفي من المال، فيمكنه استخدامه للحصول على جسم جديد وشاب ونضر. أو يستخدم بخفة، ولا يزال أفضل من الموت بالسرطان أو بمرض خطير آخر.
إذا كانت الفكرة تبدو صادمة بالنسبة لك، فيجب أن تتذكر أن رد الفعل العام الفوري على عمليات زرع القلب الأولى كان أن الأطباء كانوا "يلعبون على أنهم إله" ويستمتعون بانتهاك قوانين الطبيعة. ومن الجدير بالذكر أيضًا أنه بالنسبة للغالبية العظمى من الناس، كانت فكرة زراعة القلب أو الإخصاب في المختبر تبدو أيضًا وكأنها خيال علمي، حتى اللحظة التي تمت فيها تجربة هذه الإجراءات بنجاح، ثم أصبحت جزءًا من حياتنا. طريقة الحياة العادية[12].
ومع ذلك، لا يمكن تجاهل سؤال أخلاقي كبير وحقيقي فيما يتعلق بزراعة الرأس والدماغ: هل من العدل التبرع بجسد كامل لإنقاذ حياة شخص واحد، في حين أن نفس الجسم يحتوي على عدد كبير من الأنسجة الأخرى التي يمكن أن تكون ساعد العديد من الآخرين؟ ففي نهاية المطاف، يمكن لمتبرع واحد أن يتبرع بعينيه وكليتيه وقلبه وكبده وجلده وأعضاء أخرى. أو يمكنه أن يعطي جسدًا واحدًا فقط إلى "متبرع" واحد.
أنا على قناعة بأن هذه مسألة سيتعين علينا التعامل معها في المستقبل المنظور، لكنها لن تزعجنا لسنوات عديدة. والسبب باختصار هو الأتمتة. وفي كلمتين - إيلون ماسك.
أسس إيلون ماسك شركة Neuralink في عام 2016، بهدف تطوير واجهة من شأنها أن تتصل بأدمغة البشر وتسمح لهم بالتواصل مع الآلات - والآلات للتواصل مباشرة مع الدماغ. تقدمت الشركة بسرعة، وتمكنت بالفعل من فعل الكثير. أو قليلا يعتمد على من تسال.
إذا سألت عامة الناس، ستجد أشخاصًا يخبرونك بعيون واسعة أن نيويرلينك كان قادرًا على قراءة موجات دماغ الخنزير باستخدام أقطاب كهربائية متصلة بدماغه. سيبلغونك أن قرود Neuralink يمكنها بالفعل اللعب على الكمبيوتر دون تحريك طرف ذيلها، ناهيك عن أصابعها، ولكن من خلال الفكر وحده. تقرأ الواجهة نشاط الدماغ وتترجمه إلى تحكم بالكمبيوتر. حقا، معجزات وعجائب.
إذا تواصلت مع أطباء الأعصاب وسألتهم عن شركة Neuralink، فسوف تقابل بابتسامة معرفة. نعم، لقد نجحت الشركة بالفعل في قراءة نشاط دماغ القردة والخنازير، سيخبرونك، ثم يضيفون بشكل عرضي أن هذه أشياء قام بها العلماء في مختبراتهم بالفعل منذ عشرين عامًا. بمعنى آخر، لا جديد تحت الشمس سوى العلاقات العامة.
الحقيقة هي أن كلاهما على حق. لا تزال شركة Neuralink بعيدة كل البعد عن الابتكار في مجال علم الأعصاب، ولكننا هنا نشاهد شركة تمكنت بالفعل من النهوض من الصفر وإعادة إنتاج تجارب سبق إجراؤها في أكثر المختبرات تقدمًا في العالم وتعتمد على معرفة مخفية واسعة: كيف لعلاج القرود والخنازير، وكيفية إدخال الأقطاب الكهربائية، وكيفية إبقاء الجميع على قيد الحياة، وكيفية معالجة الإشارات والمزيد والمزيد. يمكنك القول إنها مع القرد قد انتهت تقريبًا من إعادة إنتاج ما يحدث في المختبرات، والآن يتمتع باحثوها بالمهارة والخبرة اللازمتين للمضي قدمًا.
هناك شيئان يثيران اهتمامي بشكل خاص بشأن شركة Neuralink، وكلاهما يمكن أن يكون لهما تأثير كبير على حياتنا في المستقبل. ، وكلاهما يستحق الخوض فيه للحظة.
الأول هو أن شركة نيويرلينك تنوي - في نهاية المطاف، عندما تصبح تقنيتها متقدمة بما فيه الكفاية - أن توفر للجميع طريقة للتحكم بشكل مباشر في عقولهم. وتتمثل رؤية ماسك في طبقة من الأقطاب الكهربائية التي سيتم إدخالها إلى الدماغ البيولوجي بطريقة بسيطة وبدون مضاعفات طبية، ومن خلالها نستطيع أن نخبر الدماغ بما يجب عليه فعله. ليست هناك حاجة للتقدم إلى قصص الخيال العلمي - أو الكابوسية - التي تعدنا بقدرات متقدمة على قراءة الأفكار. حتى لو تمكنا فقط من التحكم في إفراز الناقلات العصبية - السيروتونين والدوبامين وغيرها - فإن العالم سوف يتغير بين عشية وضحاها.
تخيل عالمًا مستقبليًا حيث تعود إلى المنزل متعبًا ومرهقًا من يوم عمل شاق، ولكنك لا تزال تتوق إلى كتابة الكتاب الذي طالما حلمت به. بضغطة زر واحدة، يمكنك توجيه عقلك ليكون أكثر فضولًا، وأكثر نشاطًا، وأكثر استعدادًا لنقل المعرفة إلى لوحة المفاتيح. أو ربما، على زر آخر، تسمح لنفسك بالانفتاح أكثر على مشاعرك الداخلية، وتصبح أكثر تعاطفاً وتتواصل أكثر مع زوجتك وأطفالك. الزر الثالث سيقمع جوعك، أو يزيد من قدرتك على التحكم في رغباتك لمساعدتك في اتباع نظام غذائي.
كيف يبدو لك هذا العالم؟ حلم؟ كابوس؟ كلاهما؟
في رأيي، إن الشيء العظيم في هذه الرؤية هو الاختيار الذي تمنحه لكل شخص. سيكون عليك اختيار ما هو أكثر أو أقل أهمية بالنسبة لك. سيتعين عليك أن تقرر كيفية تقسيم الوقت والاهتمام والحب بين جميع المهام والكائنات التي تحيط بنا. يريد ماسك، في الواقع، أن يمنحنا دماغًا فائقًا يمكننا استخدامه لاتخاذ قرارات بشأن أشياء كانت في السابق خاضعة إلى حد كبير لبيئتنا وبيولوجيتنا الأساسية: العواطف والحالات المزاجية.
ومرة أخرى - حلم أم كابوس؟ سوف تقرر. ربما لن تضطر إلى اتخاذ هذا القرار في العقد القادم، لكنني سأفاجأ إذا لم يكن هناك أشخاص سيستفيدون بالفعل من مثل هذا الدماغ المتفوق خلال عشرين عامًا.
النقطة الثانية المثيرة للاهتمام حول Neuralink هي أن الشركة طورت، كما تدعي، روبوتًا قادرًا على إجراء العملية المعقدة تلقائيًا لإدخال الأقطاب الكهربائية في الدماغ. ووفقا للمنشورات - التي ينبغي التعامل معها بقدر كبير من الشك - فإن الروبوت قادر حاليا على إدخال ما يقرب من مائتي قطب كهربائي في الدقيقة، باستخدام إبرة رفيعة وثقب يفتحه في الجمجمة. وبالطبع، في نهاية العملية، يقوم أيضًا بإغلاق الثقب بشكل جيد باستخدام نوع من "القابس" بحجم عملة نصف شيكل، والذي يحتوي أيضًا على جهاز إرسال تتواصل من خلاله الأقطاب الكهربائية مع البيئة.[13].

يمكن قول أشياء كثيرة عن " ماسك " - ليست كلها جيدة - لكنه يدرك أن المستقبل سوف يتشكل من خلال عدد كبير من التقنيات المختلفة التي سوف تتكامل مع بعضها البعض. على سبيل المثال، ستتمكن الروبوتات المتطورة من تقليل تكاليف زرع الأقطاب الكهربائية في الدماغ والمخاطر التي ينطوي عليها مثل هذا الإجراء. مثل هذه الروبوتات غير موجودة حتى الآن، لكن " ماسك " توقع وجودها بالفعل، وأنا أتفق معه. ومن المتوقع أن تصل الروبوتات التي تتمتع بهذا المستوى من القدرات إلى التنفيذ في العقد المقبل.
والآن فكر في الروبوتات ذات المستوى المماثل من القدرات التي ستعمل أيضًا في المختبرات والمستشفيات: الروبوتات التي يمكنها أخذ عينات الأنسجة من المرضى، وتنمية الخلايا والعناية بها في المختبرات، وطباعة الأنسجة البيولوجية - وأخيرًا أيضًا زرع الأعضاء ودخولهم إلى جسم المريض.
هل هذا المستقبل غريب جدًا بالنسبة لك؟ سنكون أكثر تحفظًا: حتى لو كان الدور الكامل للروبوتات يقتصر على زراعة الأنسجة البشرية "فقط" في المختبر، فسيظل ذلك يعني أن تكاليف استبدال الأنسجة ستنخفض بشكل كبير. إن التشغيل الآلي ــ القدرة على إنتاج الأنسجة تلقائيا ــ في أغلب الأحيان ــ من شأنه أن يضمن تمكين حتى الفقراء من الحصول على أنسجة بديلة، ما داموا يعيشون في بلد يتمتع بنظام فعّال للصحة والرعاية الاجتماعية.
لا تخطئوا: لن يحدث أي من هذا في السنوات القادمة، وربما في العقد الحالي لن نكون قادرين على إنتاج مجموعة متنوعة من الأنسجة للجميع. ولكن لتحقيق هذا الهدف العظيم الذي سيقفز بنا إلى منتصف الطريق إلى الحياة الأبدية الموعودة، يمكننا أن ننتظر ولو عقدين أو ثلاثة عقود. وحتى لو كنت لا تستطيع الانتظار حقًا، حسنًا، ليس هناك خيار آخر.
لقد عمل مهندسو الطب الحيوي منذ عقود على القدرة على استبدال الأنسجة وحتى الأعضاء الكاملة في جسم الإنسان. هناك طرق ذات إمكانات كبيرة لاستبدال الأنسجة، وأهمها طباعة الأنسجة البديلة بشكل ثلاثي الأبعاد قبل زراعتها في الجسم. ونرى أيضًا رغبة من جانب مجتمع المهندسين والمرضى في "توسيع الآفاق" واختبار قطع غيار غير عادية للجسم، مثل البنكرياس الاصطناعي الذي يتكون من ثلاثة أجزاء منفصلة - أجهزة الاستشعار والذكاء الاصطناعي ومضخة حقن الأنسولين. إن الأبحاث تتقدم بسرعة، ولكن الانتقال إلى الممارسة الطبية أبطأ، وبشكل مناسب في المجالات التي يمكن أن يؤدي فيها أي خطأ إلى خسارة حياة البشر.
يمكن أن يساعدنا الذكاء الاصطناعي والروبوتات في تسريع وتيرة البحث العلمي والتطبيق الفعلي، ولكن حتى ذلك الحين، ليس هناك شك في أنه لا يزال هناك طريق طويل لنقطعه. ومع ذلك، فأنا على قناعة بأنه في هذا القرن - وربما في العقود المقبلة - سيكون كل شخص قادرًا على الحصول على أنسجة وأعضاء تحل محل تلك التي نشأ عليها. وكما قال لي نفس أستاذ الطب: عندما نتمكن من استبدال القلب الفاشل أو الكبد الفاشل، وتجديد الجلد وتصحيح الدماغ بخلايا عصبية شابة - عندها يمكننا، في الواقع، إيقاف الشيخوخة واستعادة شباب الجميع.
إن شاء الله – قريباً في هذه الأيام.
[1] https://www.nature.com/news/2006/060403/full/news060403-3.html
[2] https://biofabexplorer.cast.org/case-stories/meet-luke
[3] https://journals.lww.com/jpojournal/FullText/2014/04000/Socket_Pressure_and_Discomfort_in_Upper_Limb.7.aspx
[4] https://www.hss.edu/condition-list_osseointegration.asp
[5] https://www.healthline.com/health-news/future-prosthetics-might-be-this-mind-controlled-bionic-arm#How-the-technology-works-compared-with-conventional-prostheses
[6] https://qz.com/2141720/modern-prosthetics-go-beyond-bionic-limbs-and-into-the-brain/
[7] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6928092/
[8] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4892160/
[9] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4892160/
[10] https://www.livescience.com/brain-organoid-optic-eyes.html
[11] https://www.bbc.com/news/magazine-37311038
[12] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6511668/
[13] https://en.wikipedia.org/wiki/Neuralink
المزيد عن الموضوع على موقع العلوم:
